雪茄煙中霉菌培養基種類篩選、計數方法適用性研究(二)
1.3試驗方法
1.3.1樣品稀釋
每個樣品各稱取25 g,用無菌剪刀剪碎,置于無菌均質袋中,加入225 mL無菌磷酸鹽緩沖液,均質器3擋均質3 min,取均質后樣液梯度稀釋,按照前期對樣品中霉菌含量的評估,依次制備4個稀釋梯度(10?1,10?2,10?3,10??)。每個樣品3次重復,進行稀釋接種。
1.3.2接種和培養
分別使用平板傾注法和平板涂布法在3種培養基上進行平行試驗,最后對3種培養基及兩種接種方式進行比較。
平板傾注法(QZ):先吸取1 mL各樣品的梯度稀釋液于培養皿中,再將20~25 mL 45℃左右的高壓蒸汽滅菌后的培養基傾倒于培養皿中。然后沿同一時針方向輕微旋轉培養皿使樣品與培養基混合均勻,待培養基完全凝固后用封口膜密封,標記后置于恒溫恒濕培養箱內于28℃±1℃正置培養。其中GB法與YC/T法需培養至第5天,Biokar法需培養至第3天。
平板涂布法(TB):吸取各樣品的梯度稀釋液于各培養基表面(每個稀釋度分別吸取0.333 mL接種量并分別加入到3塊已提前制備好的培養基平板中),后用一次性無菌L型涂布棒涂抹均勻,待培養基表面水分晾干后密封進行正置培養,培養及計數方法與平板傾注法相同。具體技術路線及方法簡稱如圖1所示。
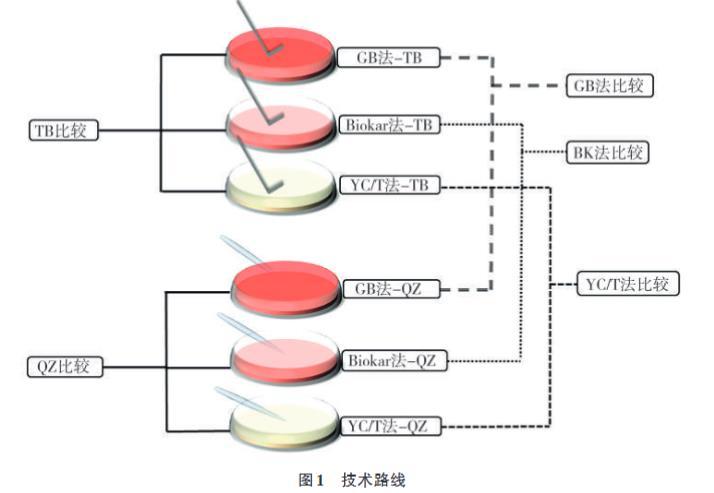
圖1技術路線
1.3.3霉菌判讀,計數及數據統計
按照各培養基特點直接肉眼觀察(必要時使用放大鏡)判別霉菌形態。
平板傾注法(最低檢出限10 CFU/g)霉菌計數公式:
霉菌含量=(∑???Q?/3)×T(1)
式中:Q?為每個重復的霉菌菌落總數;i為重復次數;T為稀釋倍數。
平板涂布法(最低檢出限10 CFU/g)霉菌計數公式:
霉菌含量=(∑???T?/3)×T(2)
式中:T?為每個重復的霉菌菌落總數;i為重復次數;T為稀釋倍數。
按照GB 4789.15—2016進行霉菌菌落計數。
1.4數據分析
使用Microsoft Excel 2010軟件進行數據整理,將所檢測霉菌計數結果轉化為以10為底數的對數值(未檢出樣品的對數值按0.7統計),采用SPSS 26.0軟件進行獨立樣本T檢驗,評價各方法對霉菌計數結果的差異顯著性。
使用Med Calc®Version 19.0.4軟件繪制Bland-Altman圖,其基本原理是計算出兩方法測量結果的一致性界限,并以圖形方式直觀反映,同時根據實際測量結果判斷兩種方法是否具有一致性。
2結果與討論
2.1霉菌計數方法比較
2.1.1 3種培養基平板涂布法的比較
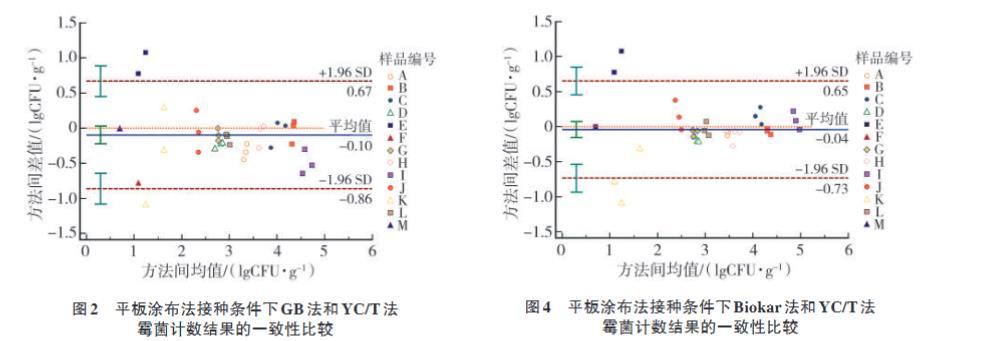
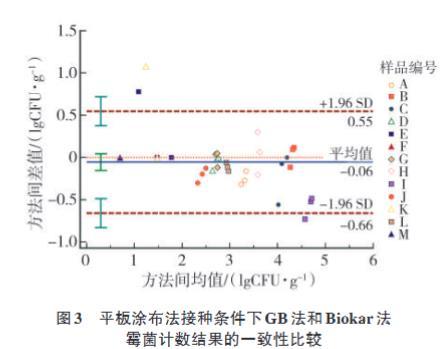
對3種培養基平板涂布法霉菌計數結果分別進行Bland-Altman圖比較,如圖2,圖3和圖4所示。將GB法-TB,Biokar法-TB和YC/T法-TB進行比較,發現除低濃度樣本中的個別數據分布在95%上下限之外,其余樣本占比分別為92.31%,92.31%和89.74%的數據點落在95%上下限內,說明3種方法間檢測結果一致性較好。當樣品中霉菌含量低于102CFU/g時,培養基對霉菌計數結果的影響較大,而當樣品中霉菌含量高于102CFU/g時,培養基對霉菌計數結果的一致性較好。表明3種培養基采用平板涂布法進行接種,對霉菌計數結果的影響與樣品中霉菌含量有關。
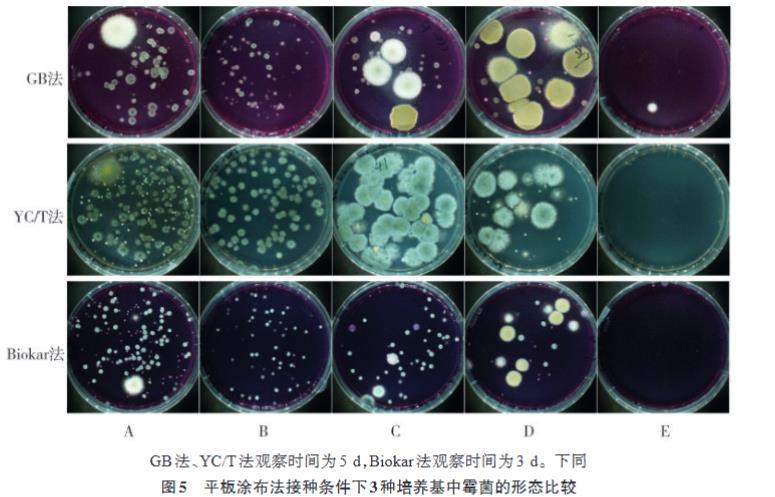
如圖5所示,通過對A,B,C,D,E等5個樣品的菌落形態觀察發現,3種培養基采用平板涂布法接種培養后樣品中典型霉菌菌落形態區別較大,其中GB法與YC/T法霉菌菌落較大,形態清晰易判讀。Biokar法典型菌落較小,分布均勻,更有助于計數,但較難從菌落形態上區分出不同種類的霉菌,由此推測Biokar法所用SYMPHONY Agar快速顯色培養基中生長促進劑和選擇性系統既可以促進霉菌的快速生長又能抑制霉菌菌絲的過度繁殖。綜合比較發現,平板涂布法接種培養基上霉菌菌落全部生長于培養基表面,GB法與YC/T法的典型霉菌菌落形態最易判別,而Biokar法更易快速計數。
2.1.2 3種培養基的平板傾注法比較
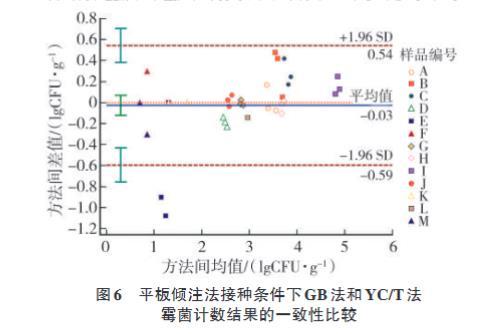
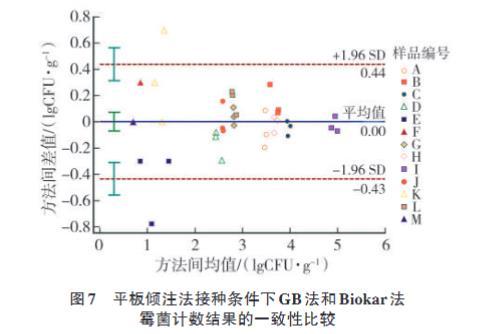
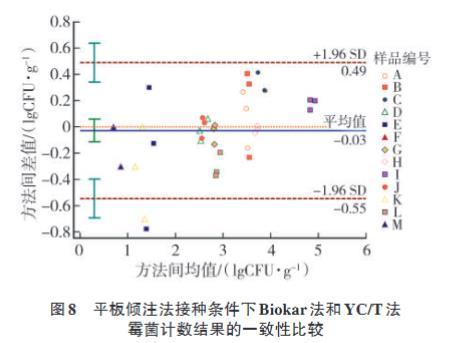
對3種培養基的平板傾注法進行分析,結果如圖6,圖7和圖8所示。從Bland-Altman圖中發現,94.87%的數據點均落在95%上下限內,表明3種培養基的平板傾注法結果一致性較好。檢測樣品中霉菌含量低于102CFU/g時,3種培養基在平板傾注法接種條件下與平板涂布法接種條件下表現出的霉菌計數結果一致。說明無論采用平板傾注法還是平板涂布法接種,當樣品中霉菌含量低于102CFU/g時,各培養基所對應的計數方法均存在一定的波動性。
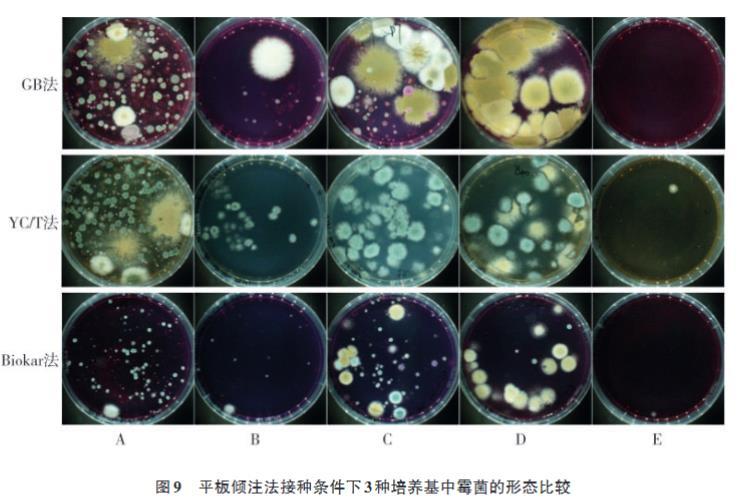
3種培養基中平板傾注法對樣品中霉菌生長狀況的影響如圖9所示。平板傾注法與平板涂布法相比,霉菌菌落除生長于培養基表面外,還在培養基內部呈現出不同的立體生長形態。YC/T法和GB法菌落生長形態相似,部分霉菌生長速率過快,菌落易蔓延,相互交錯,影響計數。Biokar法霉菌生長速率較慢,更利于霉菌計數。
