牛源解淀粉芽孢桿菌產纖維素酶活力測定、抗逆性及藥敏試驗(二)
1.3產酶條件優化
對產酶能力強的菌株進行單因素試驗:設定發酵培養基初始pH為6,接種量為1%,發酵時間分別為12、24、36、48、60 h,測定發酵時間對菌株產酶能力的影響;設定發酵培養基的初始pH為6,接種量分別為1%、2%、3%、4%、5%,發酵時間為前面得出的最佳發酵時間(48 h),測定接種量對菌株產酶能力的影響;設定發酵培養基初始pH分別為5、6、7、8、9,接種量和發酵時間為前面得出的最佳接種量(4%)和最佳發酵時間(48 h),測定發酵培養基初始pH對菌株產酶能力的影響。
1.4藥敏試驗
選擇8種抗菌藥物(氯霉素、新生霉素、阿莫西林、新霉素、慶大霉素、紅霉素、鏈霉素、利福平),以紙片法對待測菌株進行藥物敏感性測定,以了解待測菌株對抗菌藥物的耐藥性。選取藥敏紙片,按照藥敏紙片擴散法操作步驟進行相關菌株的藥敏試驗。
1.5抗逆性試驗
1.5.1人工胃液耐受性
將待測菌株接種到NB培養基中,搖瓶發酵24 h,將待測菌株發酵液按接種量10%接種于10 mL pH分別為2.0、4.0的人工胃液中處理3 h,以0 h的樣品作為對照,計算菌株存活率。
1.5.2人工腸液耐受性
將待測菌株接種到NB培養基中,搖瓶發酵24 h,取1 mL待測菌株發酵液接種到9 mL膽鹽濃度分別為0.1%、0.2%、0.3%的人工腸液中處理3 h,以0 h的樣品作對照,計算菌株存活率。
1.6體外抑菌試驗
采用瓊脂擴散法進行體外抑菌試驗。以大腸桿菌、結核桿菌、金黃色葡萄球菌作為指示菌,吸取100μL病原菌菌液,稀釋、涂布后打孔(打孔器直徑9 mm),再分別吸取待測菌株的發酵液、上清液、菌懸液100μL加入孔內,置于30℃恒溫培養箱培養1 d,重復3次,測量抑菌圈直徑,計算圈徑比(抑菌圈直徑/打孔直徑)。
1.7溶血活性試驗
以金黃色葡萄球菌為陽性對照,將待測菌株及金黃色葡萄球菌劃線接種于哥倫比亞血瓊脂培養基上,37℃培養1 d,觀察有無溶血圈產生。
1.8全基因組測序分析
采用三代測序的方法進行全基因組測序分析(委托南寧國拓生物科技有限公司完成),使用prokka工具對細菌基因組進行注釋,通過比對CAZy、GO、VFDB、CARD數據庫,對細菌基因組進行注釋。
1.9數據處理及統計學分析
用Excel 2016軟件進行數據處理,試驗結果使用GraphPad Pism 9.5軟件進行單因素方差分析及作圖。
2結果與分析
2.1目標菌株的初篩結果
根據單菌落大小、形態、顏色挑取不同形態的細菌進行純化,最終選定15株細菌。采用剛果紅染色法對選定的菌株進行初篩,得到1株能產生透明圈的菌株(圖1),將其命名為GXUN13068-1,測量其透明圈直徑為31.23 mm,菌落直徑為16.17 mm,EI為1.93。
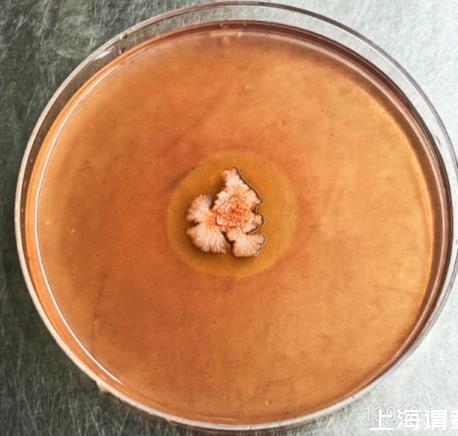
圖1菌株GXUN13068-1水解透明圈
2.2菌株鑒定結果
2.2.1菌株形態特征
菌株GXUN13068-1菌落表面有褶皺,菌落顏色為灰白色,菌落邊緣呈不規則狀,表面干燥呈磨砂樣,有火山口狀凸起(圖2-a);經革蘭氏染色,顯微鏡觀察菌體為革蘭氏陽性菌,呈藍紫色,短桿狀(圖2-b);掃描電子顯微鏡下測量菌體長約1.52μm,寬約0.65μm(圖2-c)。

圖2菌株GXUN13068-1的菌落形態(a)、革蘭氏染色(b)及掃描電子顯微鏡鏡檢形態(c)
2.2.2生理生化特征
菌株GXUN13068-1的生理生化鑒定結果生理生化鑒定結果見表1。根據鑒定結果,該菌株符合芽孢桿菌的生理生化特征。
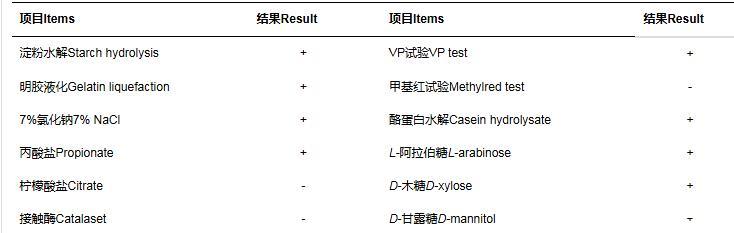
表1菌株GXUN13068-1的生理生化鑒定結果
2.2.3菌株16S rDNA的序列分析
將菌株GXUN13068-1的16S rDNA測序結果上傳至EzBioCloud進行比對分析,結果顯示,菌株GXUN13068-1與解淀粉芽孢桿菌(Bacillus amyloliquefaciens)的序列相似性為99.86%。
2.3菌株GXUN13068-1產酶發酵條件的優化結果
當發酵培養基的初始pH為6,接種量為1%時,發酵時間對菌株GXUN13068-1產酶能力的影響如圖3所示。當發酵時間為48 h時,菌株GXUN13068-1的產酶能力達到最大,所產纖維素酶活力為103.24 U/mL。
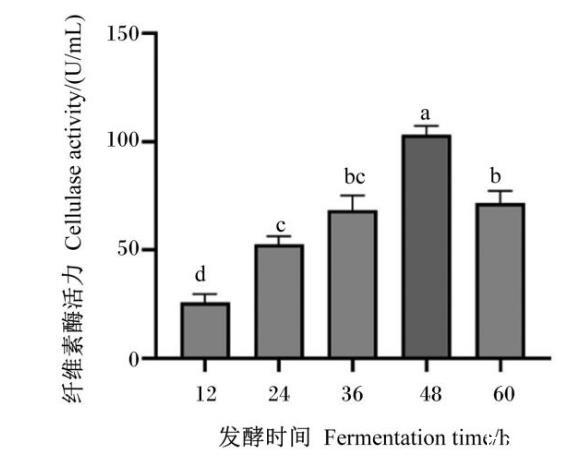
圖3發酵時間對菌株GXUN13068-1產酶能力的影響數據柱標注不同小寫字母表示處理間有顯著差異(P<0.05)。下圖同。
當發酵培養基的初始pH為6,發酵時間為48 h時,接種量對菌株GXUN13068-1產酶能力的影響如圖4所示。當接種量為4%時,菌株GXUN13068-1的產酶能力達到最大,所產纖維素酶活力為113.23 U/mL。
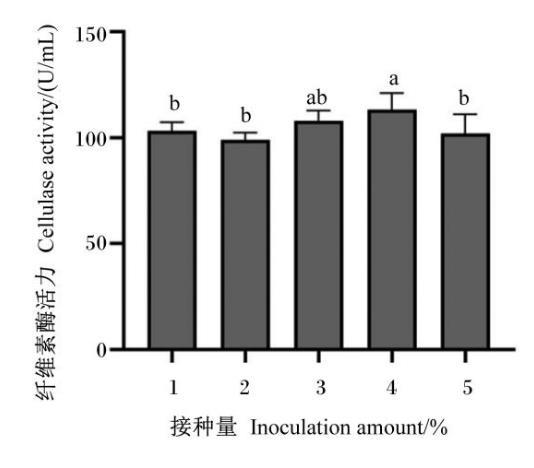
圖4接種量對菌株GXUN13068-1產酶能力的影響
當接種量為4%,發酵時間為48 h時,發酵培養基初始pH對菌株GXUN13068-1產酶能力的影響如圖5所示。當發酵培養基初始pH為9時,菌株GXUN13068-1的產酶能力達到最大,所產纖維素酶活力為126.37 U/mL。

圖5發酵培養基初始pH對菌株GXUN13068-1產酶能力的影響
2.4藥敏試驗結果
菌株GXUN13068-1對8種抗菌藥物的敏感性如圖6和表2所示。根據美國臨床標準委員會(NCCLS)的試驗要求和標準,菌株GXUN13068-1對新生霉素、慶大霉素、氯霉素、紅霉素、鏈霉素均表現為敏感,對新霉素表現為中度敏感,對利福平和阿莫西林表現出耐藥性。
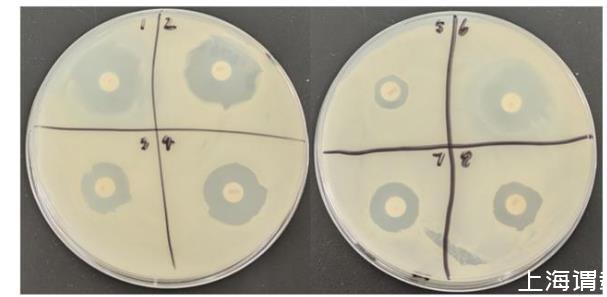
圖6菌株GXUN13068-1的藥敏試驗結果1:氯霉素chloramphenicol;2:新生霉素neomycin;3:新霉素neomycin;4:慶大霉素gentamicin;5:阿莫西林amoxicillin;6:紅霉素erythromycin;7:鏈霉素streptomycin;8:利福平rifampicin。
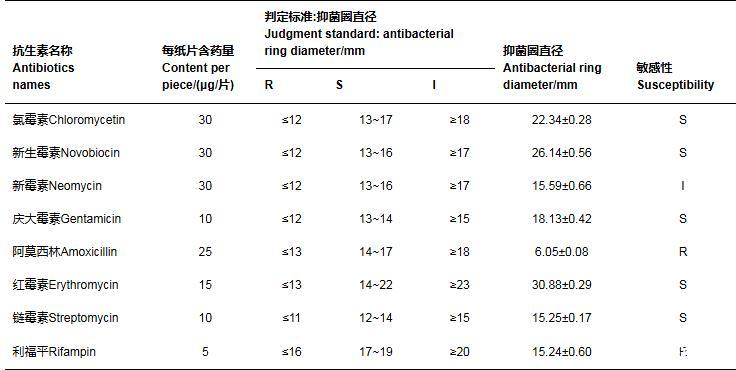
表2菌株GXUN13068-1對8種抗生素的敏感性
S:敏感;I:中介;R:耐藥。
2.5抗逆性試驗結果
2.5.1人工胃液耐受性
菌株GXUN13068-1對人工胃液的耐受性見表3。菌株GXUN13068-1的存活率隨著人工胃液pH的升高有下降趨勢,pH 2.0和pH 4.0的人工胃液處理3 h的存活率均在70%以上,說明該菌株對人工胃液具有良好的耐受性。
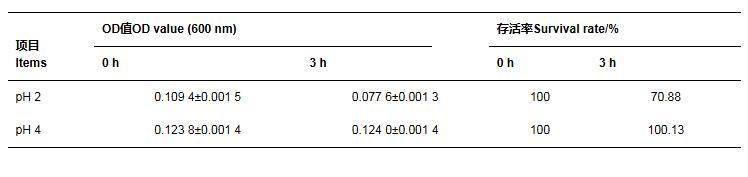
表3菌株GXUN13068-1對人工胃液的耐受性
2.5.2人工腸液耐受性
菌株GXUN13068-1對人工腸液的耐受性見表4。經膽鹽濃度分別為0.1%、0.2%、0.3%的人工腸液處理3 h后,菌株GXUN13068-1的存活率均在85%以上,說明該菌株對人工腸液有良好的耐受性。
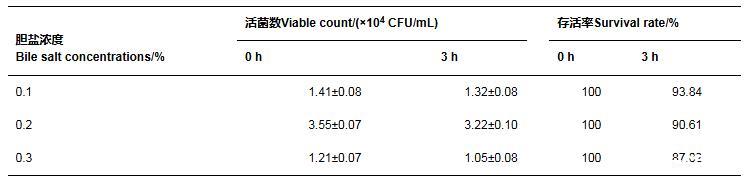
表4菌株GXUN13068-1對人工腸液的耐受性
相關新聞推薦
1、基于超微藥粉瓊脂稀釋法檢測9種致病菌對常用15種中藥的敏感性(二)
