鼻氣管鳥桿菌生長曲線測定:光電比濁法VS平板菌落計數法
為了全面解析鼻氣管鳥桿菌(Ornithobacterium rhinotracheale,ORT)的增殖特性,本研究采用雙軌并行檢測策略:一方面通過分光光度計動態監測培養液在600nm波長下的吸光度(OD600)變化,精確捕捉菌體密度波動;另一方面運用平板菌落計數法(colony-forming unit,cfu)定量分析活菌種群動態,構建雙重生長曲線進行交叉驗證。實驗數據揭示:兩種檢測方法呈現高度吻合的生長動力學特征,其中2-16小時呈現典型的指數增長趨勢(對數期),16-20小時達到生長平臺(穩定期),20小時后則進入菌體裂解階段(衰亡期)。特別針對對數期末期(16h)的定量分析表明,OD600值與活菌數存在顯著線性相關性,經最小二乘法擬合獲得精準回歸方程y=2.7591x-0.0897(R2=0.9973),該數學模型為精準調控ORT培養進程提供了量化依據。
鼻氣管鳥桿菌病作為禽類呼吸道的重要疫病,其病原體ORT可通過氣溶膠快速傳播,臨床表現為特征性呼吸困難、發育遲滯及漸進性死亡。剖檢可見典型的"三炎"病變:肺臟纖維素性化膿灶、胸膜纖維蛋白滲出及氣囊混濁增厚。值得注意的是,ORT常與禽流感病毒(AIV)、傳染性支氣管炎病毒(IBV)等形成"病原體協同網絡",通過免疫抑制效應顯著提升混合感染死亡率,據國際禽病學會統計,暴發疫情可導致禽群死亡率激增30%-50%,每年造成全球養禽業數億美元損失。該病原體最早由Devriese團隊于1994年從比利時病態火雞中分離鑒定,隨后呈現跨洲際傳播態勢,英國、以色列等15個國家相繼報道疫情。我國學者陳小玲于2003年首次分離到本土菌株,基因組測序顯示其與歐洲流行株存在顯著遺傳差異。世界動物衛生組織(OIE)最新監測數據顯示,ORT的全球流行率正以每年8.7%的速率遞增,已成為威脅禽類健康的重大病原體。
1材料與方法
1.1材料
1.1.1菌種
試驗用鼻氣管鳥桿菌由本實驗室保存。
1.1.2培養基
普通肉湯培養基(PT)、哥倫比亞血瓊脂基礎購自青島高科園海博生物技術有限公司;脫脂綿羊血,慶大霉素、多黏菌素購自杭州天和微生物試劑有限公司。
1.1.3主要儀器
紫外分光光度計(德國艾本德公司);電熱恒溫培養箱(南京實驗儀器廠);臺式全溫振蕩器(上海精宏實驗設備有限公司)。
1.2方法
1.2.1比濁法測定生長曲線
取活化后鼻氣管桿菌,接種于5mL普通肉湯培養基中,37℃,220r/min,培養16h,備用。將滅菌的普通肉湯培養基分裝于2個250mL的錐形瓶內,每瓶30mL,分為試驗組和對照組,將菌種按照1%的接種量接種于試驗組的肉湯培養基中,37℃振蕩培養。之后每兩小時取一次樣,測定試驗組與對照組在不同培養時間的OD600mm值,重復測定3次取平均值,記錄培養時間及對應OD600nm值。以OD600mm值為縱坐標,培養時間(t)為橫坐標繪制ORT生長曲線。
目前對ORT的研究集中在診斷檢測和防治技術,對于ORT的生長曲線研究報道較少。本試驗主要采用光電比濁法和平板菌落計數法來繪制ORT的生長曲線,并通過測定不同濃度菌液的OD值與活菌數構建回歸方程,研究該菌的繁殖規律。
1.2.2平板菌落計數法測定生長曲線
在5%綿羊血瓊脂培養基(5μg/mL慶大霉素,多黏菌素)傾倒于90cm平皿中,每個平皿約20mL培養基,放置于超凈臺中冷卻至凝固。將步驟1.2.1中不同時間的菌液,在超凈臺內取出200μL菌液到1.5mL無菌EP管中,且將菌液10倍遞增稀釋梯度稀釋,取10°、10°、10°三個稀釋度的菌液各200μL,在綿羊血瓊脂培養基上進行涂布,每個稀釋度菌液重復涂布三個平皿,并吸取200μL稀釋液涂布平皿做空白對照,所有平皿于37℃,5%CO2恒溫培養箱中倒置培養。培養24h后對所有的平皿進行菌落計數,計數時選取菌落數在30~300,無蔓延菌落生長的平皿,并根據公式(每毫升中菌落形成單位(cfu)=同一稀釋度三次重復的平均菌落數x稀釋倍數x5)換算出樣品中的菌落數,以菌落數(cfu)為縱坐標,培養時間(t)為橫坐標繪制鼻氣管鳥桿菌的生長曲線。
1.2.3菌液OD600nm值與菌落數(cfu)的相關性分析
挑取單菌落接種于普通肉湯培養基中,37℃恒溫振蕩器培養16h。12000r/min離心5min取菌體,用滅菌的普通肉湯培養基重懸菌液,然后進行2倍遞增稀釋,將菌液稀釋至1/2、1/4、1/8、1/16、1/32,測定不同稀釋度菌液OD600mm值并進行平板菌落計數。根據所得結果,繪制以OD600nm值為橫坐標,菌落數(cfu)為縱坐標的標準曲線。
1.2.4回歸曲線準確度驗證
將1.2.1中所測的菌液培養不同時段的OD600nm值代入標準曲線,得出理論菌落數(cfu),并繪制出曲線與平板菌落計數法測定的生長曲線進行比較驗證。
2結果
2.1 ORT的生長曲線(比濁法)

由圖1可知,在2~16h曲線呈快速增長,ORT以幾何級數生長,為對數生長期;16~20h曲線平緩,ORT總數處于穩定階段,為穩定期;20h呈曲線呈緩慢下降趨勢,ORT總數下降,為衰亡期。
2.2 ORT的生長曲線(平板菌落計數法)
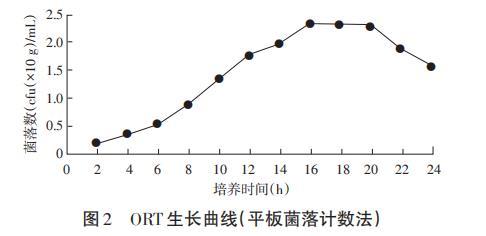
由圖2可知,ORT生長同樣分為3個時期:2~16h為對數生長期,16~20h為穩定期,20h以后為衰亡期,與比濁法所得生長曲線走向基本一致,但相對于比濁法衰亡期下降更迅速。
2.3菌液OD600nm值與菌落數(cfu)的相關性分析
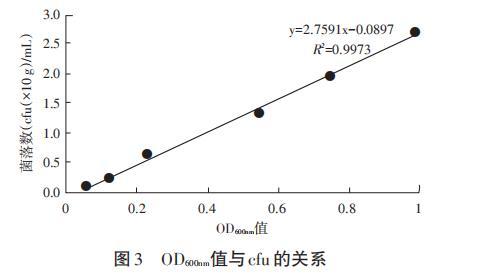
根據所測得OD600mm值及平板菌落數(cfu),以OD600mm值為橫坐標,菌落數(cfu)為縱坐標繪制的標準曲線(見圖3)。ORT對應方程為:y=2.7591x-0.0897(R2=0.9973),說明OD600mm值和菌落數(cfu)之間呈強相關性。
2.4回歸曲線準確度驗證
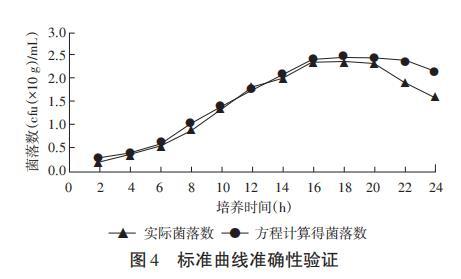
將平板菌落計數得到的菌落數(cfu)與代入方程計算得到的理論菌落數(cfu)比較,結果見圖4。由圖4可知,2~16h期間ORT的實際生長曲線與方程所得的理論曲線走勢基本重合,數值差異較小;而16h后曲線出現偏移,平板菌落計數得出的菌落數(cfu)數值明顯小于方程計算所得結果。因此該方程僅適用于ORT2~16h培養時間段內的細菌計數。
3討論
本研究通過光電比濁法及平板菌落計數法測定ORT的生長曲線,兩種方法所得生長曲線走向基本一致,由此可得出ORT的生長周期:2~16h為對數生長期;16~20h為穩定期;20h以后為衰亡期。本試驗所得的ORT生長曲線與付強等測定的A型ORT的生長曲線結果基本吻合。而后本試驗通過測定不同濃度菌液的OD值與活菌數構建回歸方程,但是該方程僅適用于對數生長期的細菌,而這個時期細菌的形態以及生物活性等都很典型,并且對外界環境的作用敏感,因此研究細菌性狀以對數生長期的細菌最好。
本試驗發現,平板菌落計數法是將菌液經梯度稀釋之后,取一定量的稀釋液接種于平皿上,在適宜條件下培養,由每個單細菌生長繁殖而形成肉眼可見的菌落,由于待測菌液往往不易徹底分散成單個細菌,長成的單菌落也可能來自2~3個或更多細菌,因此平板菌落計數的結果往往偏低。平板菌落計數法雖然操作繁瑣,試驗成本高,結果滯后,但是該方法最大優點是可以測定活菌的數量,所得結果更準確。而比濁法操作簡單,能即時獲得結果,適合連續測定,但是也存在缺點,在一定的范圍內,菌液濃度與透光度成反比,而由于在穩定期細菌代謝產物不斷累積,衰亡期細菌死亡數量增多,酶標儀所測得數值為細菌的總數,無法
區分活菌和死菌,使得衰亡期菌液的OD{}_{600text{nm}}值無明顯變化。因此,比濁法只能得出該菌各生長階段的大概時間,所得生長曲線無法普遍適用。本試驗選擇對數期的ORT,結合比濁法與平板菌落計數法,探究了OD600mm值及平板菌落數(cfu)的關系,成功構建回歸方程,綜合兩種方法優點的同時節約了時間和成本,有效地提高了ORT計數的準確性和簡便性,為下一步研究提供保障,為根據不同需要控制ORT的生長提供參考。
相關新聞推薦
1、黑曲霉中幽黑素合成途徑、生產、純化及對UV-C輻射的防護能力
2、苯乳酸對霍氏腸桿菌生長曲線、細胞凋亡、抑制活性、DNA的影響(二)
3、藜麥和藍靛果酵母菌株篩選、培養、計數及混菌液態發酵工藝優化(五)
