貝氏柯克斯體在高滲脫水環境中的生物學特性研究(三)
2.3高滲壓脫水的貝氏柯克斯體感染性VFU值的對比測定
研究表明,環境野生型與實驗室培養的貝氏柯克斯體對真核細胞的感染性不同,基于無生命培養基高滲壓脫水后的菌體對真核細胞的感染性未知。因此,我們通過qPCR定量并調整NMII10×NaCl、NMII、NMII1/100×NaCl菌體拷貝一致后,利用相差顯微鏡計數高滲脫水所得菌體NMII10×NaCl感染BGMK細胞的VFU值,可見在感染后24 h高滲透壓組菌體NMII10×NaCl的VFU較常規組NMII、低滲透壓組NMII1/100×NaCl的VFU無顯著改變。在感染后96 h,NMII10×NaCl的VFU對比感染后24 h未見明顯對數增長,這與NMII及NMII1/100×NaCl在感染后96 h VFU的對數增長顯著不同。值得注意的是,在感染后144 h,NMII10×NaCl的VFU對比感染后96 h的VFU值增加,同時與NMII有統計學差異(t=-2.11,P<0.05),這提示可能與菌體經高滲脫水處理后在胞內的適應性生長有關,如圖3所示。
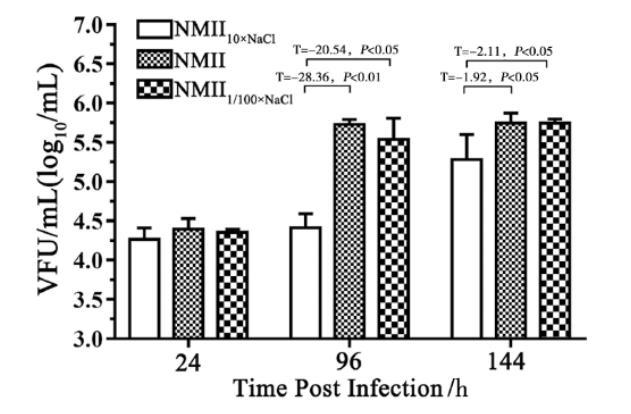
圖3滲透壓梯度培養后的貝氏柯克斯體感染BGMK細胞的VFU值
2.4透射電子顯微鏡對比分析貝氏柯克斯體菌體形態
在自然環境中,貝氏柯克斯體以耐干燥脫水且具備感染性的I相菌體廣泛存在,形態類似于雙相發育周期中直徑小于1μm的小貝氏體(SCVs)。然而在實驗室研究中,典型雙相發育周期中的大貝氏體(LCVs)直徑多大于0.5μm。使用透射電子顯微鏡觀察貝氏柯克斯體NMII10×NaCl、NMII、NMII1/100×NaCl在無生命培養環境中的形態學變化,可見脫水條件下,菌體成簇生長,直徑大多小于1μm,菌體類似脫水皺縮的表面結構。在低滲壓組中,菌體直徑大多1μm以上,形態類似于表面飽滿的球桿狀,對比可見NMII直徑約為1μm的典型菌體結構。進一步分別將NMII10×NaCl、NMII、NMII1/100×NaCl感染BGMK細胞后培養7 d,使用透射電鏡觀察可見3組菌體均可感染并在胞質內形成CCV囊泡,且囊泡直徑無明顯差別,同時菌體在CCV囊泡內呈典型的雙相發育菌體形態。這提示與無細胞培養體系中的發育周期不同,菌體在胞內的繁殖環境有利于菌體的典型雙相發育,如圖4所示。
圖4貝氏柯克斯體形態的電子顯微鏡對比分析
注:A、D為NMII10×NaCl;B、E為NM;C、F為NMII1/100×NaCl,均為培養后第7 d。
3討論
貝氏柯克斯體作為一種經氣溶膠傳播的烈性傳染病原體,具有極強的感染能力與環境抵抗力。一直以來,由于該病原自身的胞內寄生繁殖特性以及缺乏無生命克隆純化技術,關于貝氏柯克斯體的環境耐受性機制研究進展緩慢。近年來,無生命培養方法的研制不僅部分解決了貝氏柯克斯體克隆純化的難題,而且為該菌的基因編輯提供了技術支撐,同時ACCM培養基組分的可量化調整有助于實驗室模擬外界脫水條件,從而進一步探究貝氏柯克斯體的環境抵抗特性遺傳機制。
脫水是細菌失活的主要方式之一,本研究以無生命培養系統為技術平臺,成功建立了滲透壓梯度的貝氏柯克斯體脫水研究模型,為后續探究菌體耐脫水相關蛋白表達以及對應基因轉錄水平打下了基礎。我們通過研究發現貝氏柯克斯體NMII可在高達3 500 mOsm/L滲透壓脫水的無生命培養基中適應性存活,而在低滲透壓條件下可獲得有限生長,這不僅說明菌體可在無生命環境中抵抗脫水,也驗證了Na+與Cl-是無生命培養體系中實現指數增長的重要組分。另外在細胞感染及生長特性方面,在感染后96 h,經脫水后NMII10×NaCl的VFU顯著低于NMII,而低滲透壓培養的NMII1/100×NaCl與NMII在感染后96 h的VFU差別無統計學意義,但在感染后144 h,經高滲脫水后NMII10×NaCl的VFU仍較前增加,僅與NMII有統計學差異(t=-2.11,P<0.05)。這提示脫水處理后的菌體感染BGMK細胞后的適應性生長過程可能較野生型延長,同時提示上述感染及適應性生長特性改變可能與菌體生長環境中的滲透壓變化所致自身相關蛋白表達水平有關,結合菌體在透射電子顯微鏡下的形態變化,這提示這些蛋白的表達水平變化很可能影響菌體的雙相發育。
貝氏柯克斯體自然野生株的獲取及克隆制備是本領域的技術難題,一直以來缺乏實驗室研究模型,本研究成功培養制備了脫水存活的貝氏柯克斯體菌株,為進一步在蛋白質組及基因水平分析該病原耐受脫水的遺傳機制奠定了實驗性基礎。
相關新聞推薦
1、不同碳源、氮源和金屬離子對耐鋅菌株的生長特性的影響(二)
3、撒壩豬耳緣組織成纖維細胞系生長曲線、生物污染檢測結果——結果與分析、討論
