梅花鹿體細胞航天誘變、細胞樣品回收培養技術、生長曲線及核型特性(一)
摘要:本研究以自主研發的聚偏二氟乙烯膜(PVDF)細胞培養技術進行了梅花鹿(Cervus nippon)體細胞的航天培養及生物誘變,并分析了其細胞在航天誘變后的生長曲線和核型特性。采用耳緣皮膚組織塊貼壁培養的方法進行體細胞的原代培養;胰蛋白酶消化的方法完成細胞的傳代培養;依照程序降溫的方法完成細胞的冷凍保存;每天計數24孔板每孔的活細胞數并利用Excel 97-2003繪制出細胞的生長曲線,采用IBM SPSS Statistics 23統計軟件回歸分析程序中的非線性回歸分析子程序Logistic曲線模型分析細胞生長曲線的擬合度;以常規染色體標本制備技術,利用細胞遺傳工作站(AI)軟件對梅花鹿體細胞的染色體核型進行分析。
實驗結果表明,新開發的PVDF膜細胞培養技術可有效保持梅花鹿體細胞在太空飛行過程中的存活并成功回收、傳代建系。通過細胞傳代培養觀察發現,該體細胞經航天誘變后保持正常的成纖維細胞特征,生長曲線呈“S”型,航天誘變組體細胞在培養4 d進入對數生長期,與對照組體細胞在培養2 d進入對數生長期相比其細胞增殖速度減慢。擬合生長曲線分析表明,航天誘變組細胞生長擬合度值與對照組相似,但細胞增殖拐點時間、拐點細胞量分析結果證明,航天誘變后的體細胞增殖速度減慢。核型分析顯示,航天誘變梅花鹿體細胞染色體數保持2n=66,染色體形態正常,核型為66(XX),其中32對常染色體,1對性染色體。本研究建立了哺乳動物在航天運行條件下的細胞培養PVDF新技術,并分析了航天誘變對于梅花鹿細胞生物學特性變化的影響,為以后進行相關研究提供了基礎信息和技術支持。
梅花鹿(Cervus nippon)主要分布在亞洲東部,是東亞季風區特產的珍貴經濟動物之一,已列為國家Ⅰ級重點保護野生動物。梅花鹿屬于哺乳綱(Mammdia)偶蹄目(Artiodactyla)鹿科(Cervide)花鹿屬。在公元前14世紀至公元前12世紀中國就開始對野生梅花鹿進行馴養化利用,是世界上最早養殖梅花鹿的國家。我國作為目前世界上僅有的3個(美國、俄羅斯、中國)掌握返回式衛星技術的國家之一,近些年來在航天生物育種領域取得了一系列開創性研究成果。2016年4月6日凌晨升空的“實踐十號”衛星,搭載了來自內蒙古賽科星家畜種業與繁育生物技術研究院提供的牛(Bos taurus)、綿羊(Ovis aries)、梅花鹿等大型動物和野生動物的體細胞(somatic cell)、精子(sperm)等材料,這是我國首次在太空進行大型動物航天生物誘變實驗。
本研究以雌性梅花鹿體細胞為材料,開發了哺乳動物體細胞在太空的培養新技術,與對照組比較分析了航天誘導的梅花鹿體細胞的細胞生長、染色體變化等生物學特性,為動物的航天生物育種技術建立提供了基礎資料和相關信息。本研究同時對于豐富我國動物品種資源庫、提升梅花鹿產業競爭力具有重要戰略性意義。
1材料與方法
1.1實驗材料
2016年3月在內蒙古賽科星家畜種業與繁育生物技術研究院實驗基地選取19月齡健康的雌性梅花鹿,編號為NCH32,剪取其耳緣皮膚組織用于實驗。
1.2雌性梅花鹿NCH32成纖維細胞系的建立
剪取雌性梅花鹿NCH32的耳緣皮膚組織約1 cm2,用手術刀片剔除耳毛,并用含有青霉素和鏈霉素雙抗的PBS清洗3次,24 h內送回實驗室進行原代細胞建系培養。在超凈工作臺中,用75%酒精浸泡采取的組織樣品30 s,再用Dulbecco磷酸鹽緩沖液(Dulbecco′s phosphate buffered saline,DPBS)(GIBCO公司)沖洗3次,用手術刀片剔除皮膚間的結締組織,將其剪成1 mm3左右的小塊,用無菌玻璃管將組織碎塊均勻分布于培養瓶中,加入5 ml含有10%胎牛血清(fetal bovine serum,FBS)(GIBCO公司)的MEM-Alpha(1×)(α-MEM)培養液(GIBCO公司),在37.5℃、5%CO?的培養箱(RS Biotech 311)中倒置培養4~6 h后,正置培養瓶繼續培養。連續培養12 d以后,耳皮成纖維細胞生長至約90%匯合度時,按常規方法傳代培養。棄去原有培養液,用DPBS沖洗細胞后,加入0.25%胰蛋白酶(Sigma公司)消化2~3 min。細胞脫壁后加入含10%FBS的α-MEM培養液終止消化。離心并收集細胞,按照1︰3比例分瓶傳代培養。成纖維細胞傳至6~8代時用于染色體標本制備。
1.3梅花鹿體細胞的航天培養方法
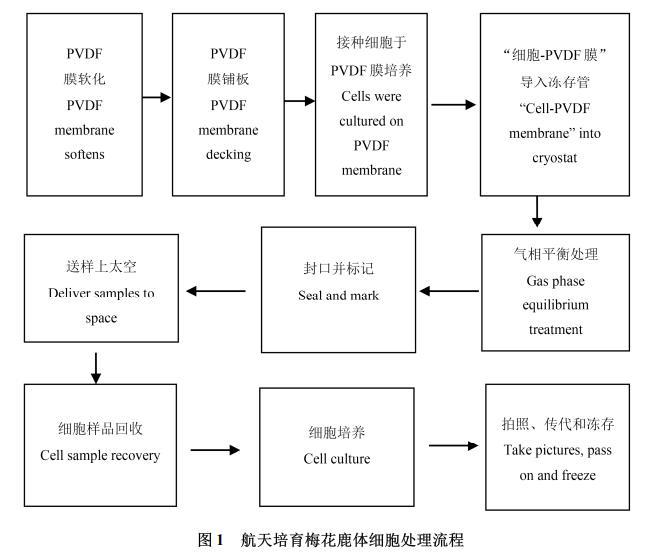
根據實驗經費和實驗材料的特殊性,此次實驗按照本實驗室自主研發的新型成纖維細胞在太空環境的聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)培養方法,將梅花鹿體細胞搭載于實踐10號返回式科學實驗衛星上,并在太空中飛行12 d后進行回收、培養和保存。具體實驗方法參照用于航天生物育種的家畜成纖維細胞培養方法(內蒙古賽科星家畜種業與繁育生物學技術研究院有限公司2016),實驗流程見圖1。
1.3.1培養基配制
實驗中共使用了2種培養基,具體配制方法如下。
1×液體培養基:5 ml胎牛血清(FBS),0.5 ml青霉素/鏈霉素雙抗,用MEM-Alpha(1×)培養液定容至50 ml。
瓊脂固體培養基:首先配制1%瓊脂,稱取5.0 g瓊脂并加入50 ml蒸餾水,微波爐加熱融化后,進行高壓滅菌。之后配制2×液體培養基:20 ml胎牛血清(FBS),1 ml青霉素/鏈霉素雙抗,1 ml非必須氨基酸(essential amino acid,NEAA),用2×MEM定容至50 ml。最后,將1%瓊脂滅菌后冷卻至40℃左右,與38℃預熱的2×液體培養基按1︰1混合配制成0.5%瓊脂固體培養基。
相關新聞推薦
1、不同碳源、氮源、培養溫度、PH值對褐藻酸降解菌AGN12菌生長及產酶的影響
