鴨瘟病毒基因缺失株rDEV-ΔVP26生長曲線、蝕斑面積及免疫原性分析(三)
2.3重組病毒的一步生長曲線
測定重組病毒rDEV-ΔVP26和親本毒株rDEV-EF1在CEFs上的一步生長曲線并進(jìn)行比較,如圖4所示,rDEV-ΔVP26株和rDEV-EF1株具有相似的增殖趨勢。rDEV-ΔVP26株的滴度在接種CEFs后穩(wěn)步增加,到84 h時達(dá)到峰值,病毒滴度為105.36 TCID50·0.1 mL-1。rDEV-EF1穩(wěn)步增加到60 h達(dá)到峰值,病毒滴度為105.6 TCID50·0.1 mL-1。在此期間rDEV-ΔVP26滴度較親本毒株rDEV-EF1有所降低,說明UL35基因缺失會輕微影響病毒增殖,并降低病毒滴度。
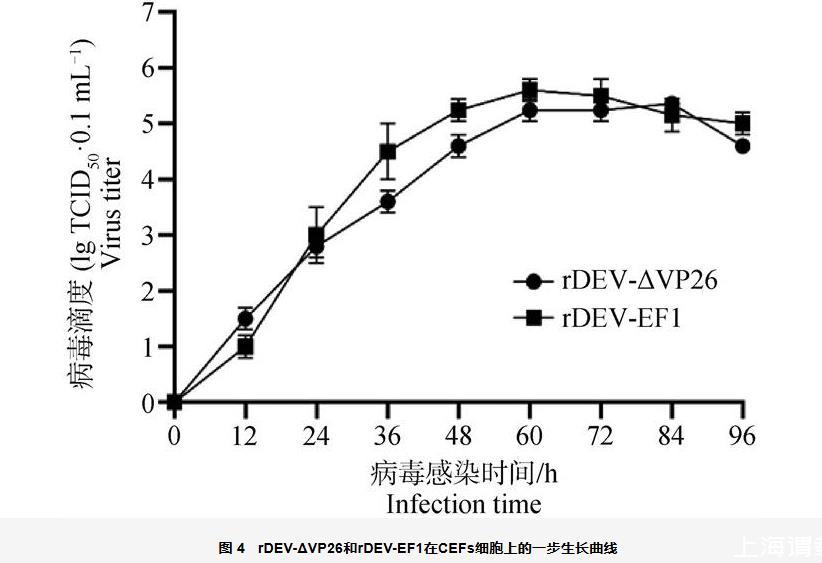
圖4 rDEV-ΔVP26和rDEV-EF1在CEFs細(xì)胞上的一步生長曲線
2.4重組病毒蝕斑面積測定
rDEV-EF1和rDEV-ΔVP26感染細(xì)胞48 h,各拍攝病毒蝕斑照片100個,并用ImageJ軟件測量各個蝕斑面積并計算平均值。發(fā)現(xiàn)rDEV-ΔVP26蝕斑面積較rDEV-EF1減少10.60%(P<0.05)(圖5)。

圖5基因缺失病毒rDEV-ΔVP26和對照病毒rDEV-EF1在CEFs細(xì)胞上的蝕斑面積測定和比較
2.5 UL35基因缺失病毒的安全性分析
各組免疫后觀察2周,發(fā)現(xiàn)各劑量的rDEV-ΔVP26組、rDEV-EF1組和DMEM對照組鴨子精神狀態(tài)良好,均未出現(xiàn)死亡(表2)。
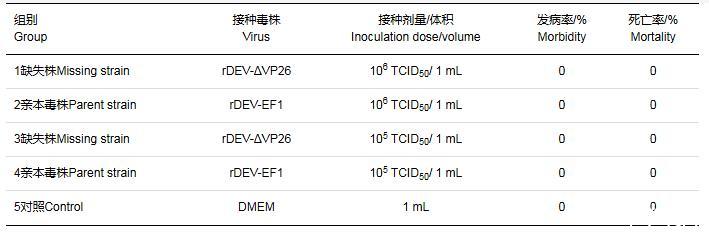
表2不同劑量rDEV-ΔVP26免疫鴨對鴨子的安全性試驗
2.6 UL35基因缺失病毒的免疫原性分析
在免疫rDEV-ΔVP26或rDEV-EF1 14 d后,用同一劑量的DEV CHv株(100 DLD50)進(jìn)行攻毒,于2周內(nèi)觀察鴨的發(fā)病和死亡情況(圖6),發(fā)現(xiàn)1×104 TCID50的rDEV-ΔVP26免疫組鴨在攻毒5 d后死亡2只,保護(hù)率為75%;1×104 TCID50 rDEV-EF1免疫組鴨在攻毒后5 d死亡1只,保護(hù)率為87.5%;1×105 TCID50 rDEV-ΔVP26免疫組鴨和1×105 TCID50 rDEV-EF1免疫組鴨無死亡,保護(hù)率為100%。DMEM對照組鴨在攻毒后全部發(fā)病并死亡,其中第4天死亡1只,第5天死亡6只,第6天死亡1只。正常對照組試驗期間全部存活。對各組鴨的存活率進(jìn)行統(tǒng)計,注射1×105 TCID50 rDEV-ΔVP26組的存活率與親本對照組rDEV-EF1保護(hù)率相同,均為100%。注射1×104 TCID50 rDEV-ΔVP26組的存活率較親本對照組rDEV-EF1下降12.5%。該研究結(jié)果表明,1×105 TCID50的rDEV-ΔVP26免疫麻鴨后,誘導(dǎo)針對DEV強(qiáng)毒株的免疫保護(hù)能力與親本疫苗株相同。
分別用兩種劑量(1×104 TCID50和1×105 TCID50)的rDEV-ΔVP26和對照毒株rDEV-EF1免疫鴨后14 d,用DEV強(qiáng)毒株對免疫鴨進(jìn)行攻毒,統(tǒng)計鴨的存活率。
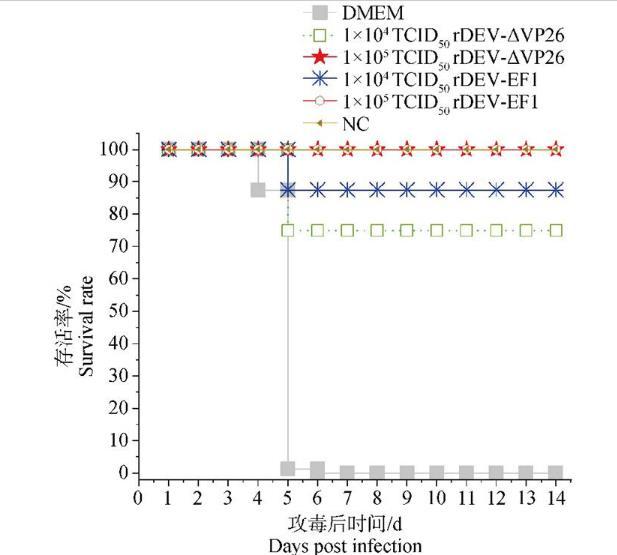
圖6 rDEV-ΔVP26的免疫保護(hù)效果
3討論
鴨瘟是鴨、鵝和其他雁形目禽類的一種急性、熱性、敗血性疾病。尚無有效的治療藥物,預(yù)防接種仍是防控DEV的主要手段。目前,市場上在售疫苗主要以傳統(tǒng)疫苗為主,包括滅活疫苗和弱毒疫苗。滅活疫苗成本高、副反應(yīng)大,也存在滅活不徹底的風(fēng)險。DEV雞胚化減毒活疫苗免疫效果好,但是存在毒力返強(qiáng)和隱性帶毒等安全隱患。通過疫苗免疫曾控制了DEV的流行,但目前鴨瘟疫情存在死灰復(fù)燃之勢。近年來,在山東、江西、河北、江蘇、河南、安徽、湖北、福建、廣西等地蛋鴨、櫻桃谷肉鴨、種鴨、番鴨均出現(xiàn)了新型鴨瘟疫情。雖然新型鴨瘟與傳統(tǒng)鴨瘟,在鴨的解剖病變與癥狀方面存在許多相同之處,但是新型鴨瘟傳播速度更快、致死率和死亡率更高,且在雛鴨開始發(fā)病。因此,亟需一種更安全有效的新型疫苗,既可進(jìn)行有效防控,又能從病毒基因組水平與抗體水平將疫苗接種與野毒感染鴨區(qū)分,從而開展鑒別診斷,對感染鴨及時有效地進(jìn)行淘汰。
目前,通過檢測DEV UL2、LORF5基因能區(qū)分免疫的疫苗株和強(qiáng)毒株,但疫苗免疫后抗體水平的監(jiān)測缺乏有效的評估手段。而且研究表明由雞胚傳代致弱的DEV疫苗株對雞群是致死的,因此接種DEV疫苗株的鴨群對于混養(yǎng)的雞群來說存在安全隱患。DEV VP26被證實與病毒致病性相關(guān),UL35基因缺失株相比于DEV疫苗株理論上安全性更好。
在α-皰疹病毒中,比較成功的案例是偽狂犬病病毒(pseudorabies virus,PRV)基因缺失疫苗,缺失的靶標(biāo)集中于非必需的毒力相關(guān)基因,如tk、US8(gE)、US7(gI)、US4(gG)等,PRV TK-/gE-弱毒疫苗,很早以前已經(jīng)廣泛應(yīng)用于美國、歐盟等啟動PRV根除計劃的國家;PRV gE-/gI-弱毒疫苗,由中國農(nóng)業(yè)科學(xué)院哈爾濱獸醫(yī)研究所引進(jìn)、國內(nèi)推廣應(yīng)用多年、安全記錄良好;由四川農(nóng)業(yè)大學(xué)郭萬柱等研發(fā)的PRV TK-/gE-/gI-三基因缺失病毒和由華中農(nóng)業(yè)大學(xué)陳煥春團(tuán)隊研發(fā)的PRV TK-/gG-獲得新獸藥證書。這些成功的案例給人們研發(fā)鴨瘟病毒基因缺失疫苗提供了借鑒。迄今為止,多株鴨瘟病毒基因缺失株已被構(gòu)建成功,并對其免疫保護(hù)能力進(jìn)行了評估,如鴨瘟病毒ICP27、UL47、US3、UL44(gC)/gE、UL44、US10基因缺失株,都取得了不錯的效果,但還沒到應(yīng)用的階段。
本研究首次將目標(biāo)瞄準(zhǔn)衣殼蛋白,嘗試研究最小衣殼蛋白缺失對病毒的影響,發(fā)現(xiàn)DEV UL35缺失對其病毒疫苗株安全性沒有影響,但病毒傳播能力和滴度都有輕微的降低,低劑量(1×104 TCID50)rDEV-ΔVP26的免疫保護(hù)能力較對照組有所下降,但高劑量(1×105 TCID50)組無差別,這個劑量與市售的一羽份鴨瘟活疫苗劑量(107.7copies·只-1,即105 TCID50)相當(dāng)。對于rDEV-ΔVP26作為鑒別診斷基因缺失疫苗的可行性,筆者進(jìn)行了初步評估,后續(xù)還需要開展更多的研究,如病毒接種最低劑量、接種途徑、對雞群的安全性、配套的基于VP26蛋白的間接ELISA檢測技術(shù)等。
4結(jié)論
本研究在鴨瘟病毒疫苗株感染性克隆的基礎(chǔ)上,構(gòu)建了UL35基因缺失的病毒株rDEV-ΔVP26。高劑量rDEV-ΔVP26接種鴨體安全性良好,且1×105 TCID50滴度的rDEV-ΔVP26免疫組在強(qiáng)毒攻擊下的保護(hù)率與相同劑量的rDEV-EF1對照組一致。該研究為研發(fā)用于區(qū)分疫苗免疫和野毒感染的DEV鑒別診斷疫苗奠定了基礎(chǔ)。
相關(guān)新聞推薦
2、優(yōu)化培養(yǎng)基配方減少無機(jī)硒對粗毛纖孔菌的抑制作用,同時提高富硒菌絲的產(chǎn)量(二)
3、快速藥敏檢測技術(shù)方法、原理、臨床轉(zhuǎn)化需求(一)
