Mg2?對嗜酸氧化亞鐵硫桿菌生長、氧化活性的影響規律——結果與討論、結論
2結果與討論
2.1 Mg2?質量濃度對體系pH值的影響
細菌氧化過程伴隨著H?及電子的移動,從而導致pH值改變。不同Mg2?質量濃度下At.f菌培養過程中pH值隨時間的變化情況如圖1所示。
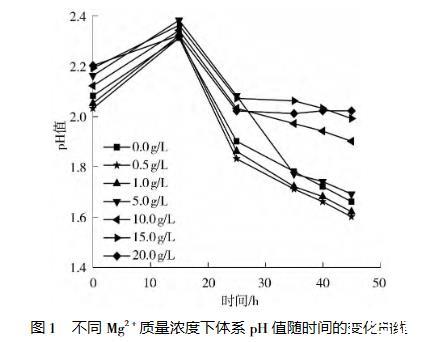
從圖1中可以看出,整個培養過程中體系pH值呈先升高后逐漸下降的趨勢。這是因為在培養初期,氧化亞鐵硫桿菌氧化Fe2?為Fe3?,消耗大量H?,從而導致體系pH值升高;隨著培養過程的進行,Fe3?發生水解使培養體系酸度增加,導致體系pH值下降。Mg2?的存在使得體系pH值隨時間的變化趨勢發生了較大變化,當Mg2?質量濃度≤1.0 g/L時,pH值下降速度較快,在45 h時Mg2?質量濃度為0.0、0.5、1.0 g/L的體系pH值分別下降到1.66、1.60、1.62;而當Mg2?質量濃度≥5.0 g/L時,pH值下降較慢,在45 h時Mg2?質量濃度為20.0 g/L的體系pH值僅下降到2.02。
2.2 Mg2?質量濃度對體系Eh值的影響
氧化還原電位能從整體上反映系統的氧化能力。不同質量濃度Mg2?下At.f菌培養過程中Eh值隨時間的變化情況如圖2所示。
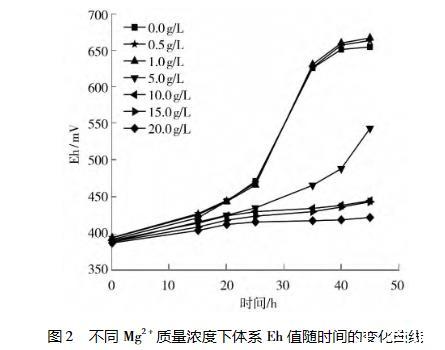
從圖2可以發現:體系的Eh值隨培養時間的延長呈先逐漸升高后趨于穩定的趨勢。在細菌生長過程中,Fe2?的氧化為細菌生長提供所需能量,使得溶液中Fe3?濃度增加,溶液的混合電位逐漸升高;當Fe2?氧化完全時,氧化還原電位達到最高值,且維持在相對穩定的范圍內。Mg2?對體系Eh值影響較大,當Mg2?質量濃度≥5.0 g/L時,體系中電位上升較慢,Mg2?質量濃度超過10.0 g/L時體系的Eh值在整個45 h的培養過程中都處于較低水平,最高僅可達440 mV左右;而當Mg2?質量濃度<5.0 g/L時,體系的Eh值在35 h左右均已達到600 mV以上,說明小于5.0 g/L的Mg2?質量濃度對At.f菌氧化活性沒有負面影響。
2.3 Mg2?質量濃度對體系Fe2?氧化率的影響
Mg2?質量濃度對At.f菌氧化活性的影響見圖3。
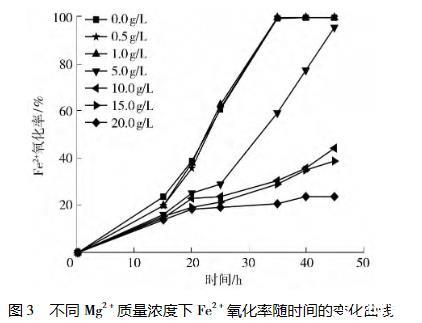
圖3表明:Mg2?質量濃度<5.0 g/L時,在35 h后Fe2?氧化率均接近100%,且在Mg2?質量濃度為1.0 g/L時,培養25 h后Fe2?氧化率達到62.78%,高于不添加Mg2?時的Fe2?氧化率(60.73%),說明適當的Mg2?能夠提高細菌的氧化活性;隨著Mg2?質量濃度繼續升高,Fe2?氧化率逐漸降低,Mg2?質量濃度為5.0、10.0、15.0、20.0 g/L時培養45 h后Fe2?氧化率才分別達到95.47%、44.31%、38.80%、23.74%,說明Mg2?質量濃度超過5.0 g/L時,細菌的氧化活性顯著降低。
2.4 Mg2?質量濃度對At.f菌生長的影響
不同質量濃度Mg2?作用下At.f菌的生長情況如圖4所示。

從圖4中可以看出:Mg2?質量濃度≤1.0 g/L時,細菌生長速度快,達到對數生長期的時間短,且隨著離子質量濃度的增加,細菌濃度也增大,說明適量的鎂離子能夠促進細菌的生長;當Mg2?質量濃度超過1.0 g/L時,細菌生長受到抑制,延滯期增長,5.0、10.0 g/L Mg2?質量濃度條件下,均在40 h才達到細菌生長旺盛期,且Mg2?濃度越大,細菌濃度越低;當Mg2?質量濃度繼續增大到15.0、20.0 g/L時,整個培養過程中,細菌濃度都偏低,說明此時細菌生長受到抑制。這是因為,Mg2?質量濃度過高導致細菌體內與溶液之間的滲透壓增加,從而影響其正常的生理功能,或者影響其他物質代謝過程的進行,包括阻礙其他物質進入細胞、影響其他酶的代謝功能等,從而導致細菌的正常生長受到抑制。
2.5 Mg2?作用前后細菌的表面電位分析
At.f菌在Mg2?質量濃度為0.0、20.0 g/L體系中培養后,其表面電位隨pH值的變化曲線如圖5所示。

從圖5中可以發現,At.f菌在Mg2?質量濃度為0.0 g/L體系中生長時的等電點為2.7,而在Mg2?質量濃度為20.0 g/L體系中生長時的等電點為3.6。等電點能指示一些官能團如羧基(—COOH)、氨基(—NH)和羥基(—OH)的存在,這些官能團存在于胞外多聚物中,并且決定細胞表面帶何種電荷,因此At.f菌在不同生長條件下等電點的不同說明其胞外多聚物存在較大差異。等電點在pH=2.0~2.8之間說明細胞表面主要含葡萄糖酸或含其他與羧基相關的多糖,等電點在pH≥3.2時說明其細胞壁表面主要為蛋白質。這說明,高濃度Mg2?的存在使得細菌細胞壁表面成分發生了改變,這可以從宏觀上解釋細菌氧化活性降低的原因。
2.6 Mg2?作用前后細菌紅外光譜分析
Mg2?作用前后的細菌經冷凍干燥處理后可進行紅外光譜掃描,通過對比作用前后細菌表面官能團的變化情況,能夠定性得出Mg2?對細菌的作用。At.f菌在0.0、20.0 g/L Mg2?中培養后細菌表面的紅外光譜圖見圖6。
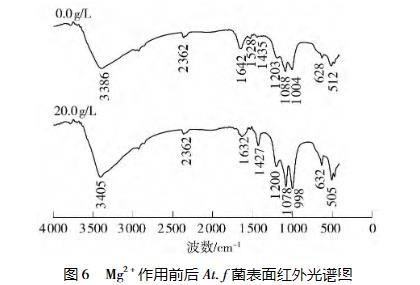
由圖6可以看出:細菌在20.0 g/L Mg2?培養體系中,3386 cm?1處蛋白質的—OH伸縮振動吸收峰偏移到了3405 cm?1處;1642 cm?1處酰胺I峰(蛋白質肽鍵)的—C=O伸縮振動吸收峰偏移到了1632 cm?1處,且峰形有所減弱;1528 cm?1處酰胺I峰蛋白質肽鍵的N—H彎曲振動吸收峰明顯消失;1435 cm?1處的波峰為附近的蛋白質分子中—CH?反對稱變形振動和—CH?中等強度對稱變形振動的吸收重疊峰,偏移到了1427 cm?1處,且峰形有明顯的增強;1203 cm?1處的—C=O彎曲振動和O—H彎曲振動峰略有加強;1088 cm?1處磷酰基的—P=O伸縮振動峰偏移到1078 cm?1處;1004 cm?1處的弱到中等強度—CN伸縮振動吸收峰偏移到了998 cm?1處,且峰形明顯增強;628和512 cm?1處的多糖—CH?吸收峰也有所偏移。造成上述現象的原因可能是Mg2?濃度過高,細菌細胞壁表面的—OH、—C=O、—CH?、—CH?、—P=O、—CN、N—H等基團發生了交聯作用。
綜上所述,高濃度Mg2?對細菌氧化活性的抑制機理在宏觀上表現為菌體表面Zeta電位的變化,在微觀上表現為對細菌細胞壁結構的破壞。高濃度Mg2?作用下,細菌細胞壁成分中的—OH、—C=O、—CH?、—CH?、—P=O、—CN、N—H等官能團發生交聯反應,一方面破壞了細胞壁的骨架結構,另一方面改變了這些基團的電離或水解平衡,使細菌表面所帶電荷大小發生變化,繼而引起菌體表面Zeta電位變化,從而抑制了細菌的生長,降低了細菌的氧化活性。
3結論
文中探討了Mg2?質量濃度對At.f菌氧化活性的影響,發現:Mg2?質量濃度<5.0 g/L時,能夠促進細菌生長,提高細菌的氧化活性,在培養35 h時,體系的pH值均下降至1.70左右,Eh值均達到600 mV以上,Fe2?氧化率均接近100%,細菌生長達到旺盛期;但Mg2?質量濃度超過5.0 g/L時,細菌濃度、氧化活性隨Mg2?質量濃度增加而逐漸降低,培養45 h后,Mg2?質量濃度為20.0 g/L體系的pH值為2.02,Eh值僅為420 mV,Fe2?氧化率僅為23.74%。研究還發現,20.0 g/L Mg2?對細菌氧化活性的抑制機理在宏觀上表現為菌體表面Zeta電位的變化,等電點由2.7變為3.6;在微觀上表現為細菌細胞壁的—OH、—C=O、—CH?、—CH?、—P=O、—CN、N—H等官能團發生了變化。
