貝氏柯克斯體在高滲脫水環(huán)境中的生物學(xué)特性研究(二)
1.3基因組拷貝數(shù)變化與生長曲線的測定
分別于培養(yǎng)周期第0 d與第7 d收取已接種貝氏柯克斯體的高滲壓組(ACCM+10×NaCl)、常規(guī)組(ACCM-2)及低滲組(ACCM+1/100×NaCl)培養(yǎng)基,后用試劑盒提取NMII10×NaCl、NMII、NMII1/100×NaCl基因組DNA,通過Taqman探針法進(jìn)行實時熒光定量PCR測定培養(yǎng)前后各組dotA基因拷貝數(shù)變化情況,做柱狀圖并以t檢驗統(tǒng)計分析組間差異。分別收集培養(yǎng)周期中第0 d至第7 d的貝氏柯克斯體菌液,提取基因組DNA后以熒光定量PCR測定dotA基因拷貝數(shù)并計算標(biāo)準(zhǔn)差,以折線圖描記生長曲線。熒光定量PCR反應(yīng)條件設(shè)定為:95℃預(yù)變性10 min,94℃變性15 s后60℃退火1 min共40個循環(huán),PCR擴(kuò)增曲線R2值均為99%以上,且P<0.05,實驗所需引物及探針序列如表2。

表2熒光定量PCR反應(yīng)所需引物及探針序列
1.4貝氏柯克斯體BGMK細(xì)胞的感染與VFU的測定
在培養(yǎng)周期第7 d分別離心收取ACCM+10×NaCl、ACCM-2及ACCM+1/100×NaCl培養(yǎng)所得菌體NMII10×NaCl、NMII、NMII1/100×NaCl,用試劑盒提取基因組DNA后以qPCR定量測定菌體拷貝數(shù)。將新傳代的BGMK細(xì)胞經(jīng)細(xì)胞計數(shù)板精確計數(shù)后接種24孔培養(yǎng)板后置于5%CO2,37℃培養(yǎng)箱靜置培養(yǎng)形成細(xì)胞單層,以感染復(fù)數(shù)(MOI,Multiplicity Of Infection)5:1的比例加入菌體后以300 g離心感染30 min,將已感染的細(xì)胞在RPMI1640培養(yǎng)基以及37℃,5%CO2培養(yǎng)箱種靜置培養(yǎng)7 d。用倒置相差顯微鏡在200×放大倍數(shù)下分別觀察計數(shù)NMII10×NaCl、NMII、NMII1/100×NaCl感染細(xì)胞后的囊泡數(shù)量,即集落形成單位(VFU,Vacuole Forming Units),分別計算并作柱狀圖統(tǒng)計分析,進(jìn)一步在400×倍數(shù)放大下觀察囊泡內(nèi)菌體形態(tài)。
1.5透射電子顯微鏡技術(shù)對比分析菌體形態(tài)
取經(jīng)qPCR定量后的貝氏柯克斯體菌體NMII10×NaCl、NMII、NMII1/100×NaCl,用PBS清洗5遍后將菌液樣品先后置于50%至100%梯度濃度的丙酮溶液中脫水1 h,將樣品包埋多孔橡膠包埋模板中形成包埋塊,乙酸雙氧鈾染色4 h,后用Hitachi H-7600透射電子顯微鏡觀察并拍照記錄。相似的,用細(xì)胞刮刀收取貝氏柯克斯體感染后第7 d的BGMK細(xì)胞,經(jīng)磷酸-戊二醛溶液充分固定后,按照文獻(xiàn)報道的操作步驟SOP進(jìn)行脫水、浸透包埋并制作超薄切片后用Hitachi H-7600透射電鏡觀察記錄并對比分析菌體形態(tài)。
2結(jié)果
2.1貝氏柯克斯體可耐受高滲透壓無細(xì)胞培養(yǎng)環(huán)境并存活
無生命培養(yǎng)系統(tǒng)的建立,不僅為該菌的克隆純化與遺傳學(xué)操作提供了全新技術(shù)工具,也進(jìn)一步揭示了該菌繁殖生長的必需條件。研究發(fā)現(xiàn)在ACCM-2液體培養(yǎng)基中終濃度125 mmol/L的NaCl有助于該菌基因組實現(xiàn)2倍log10以上的增長,同時Na+及Cl-也是無生命培養(yǎng)體系中滲透壓的主要決定因素。我們通過如表1所示10倍增加ACCM-2培養(yǎng)基中的NaCl終濃度至125 mmol/L改變菌體生長環(huán)境中的滲透壓條件,使菌體在單個培養(yǎng)周期中持續(xù)脫水,同時10倍減低NaCl終濃度至1.25 mmol/L使菌體在低滲壓下連續(xù)培養(yǎng)7 d。倒置相差顯微鏡下初步觀察見菌體形態(tài)較常規(guī)培養(yǎng)菌體相比,以散在的細(xì)小球桿狀為主,其形態(tài)類似于該菌雙相發(fā)育周期中的小貝氏體(SCVs)。進(jìn)一步以菌體NMII10×NaCl、NMII、NMII1/100×NaCl感染BGMK細(xì)胞后連續(xù)觀察,鏡下放大(400×)后可見NMII10×NaCl感染細(xì)胞后12 h可正常形成繁殖囊泡(CCV),菌體正常生長并在7 d后可見充滿菌體的CCV囊泡,對比常規(guī)組及低滲壓組,可見已形成的囊泡形態(tài)無明顯差別,菌體在囊泡內(nèi)正常生長,如圖1。這說明貝氏柯克斯體可耐受高滲壓的無生命培養(yǎng)環(huán)境并適應(yīng)性存活7 d以上,同時提示無生命培養(yǎng)環(huán)境中的高滲透壓條件可能并未顯著影響細(xì)菌對真核細(xì)胞的感染能力。

圖1梯度滲透壓培養(yǎng)后的貝氏柯克斯體感染BGMK細(xì)胞
注:A為NMII10×NaCl;B為NMII;C為NMII1/100×NaCl,均為感染后第7 d
2.2貝氏柯克斯體在高滲壓無生命培養(yǎng)環(huán)境下基因組拷貝無明顯改變且菌體未生長
據(jù)報道,貝氏柯克斯體基因組可在ACCM系列培養(yǎng)基中完成(2~4)log10的增長,而在自然界中該菌可耐受干燥脫水適應(yīng)性存活并廣泛傳播。因此,在以ACCM-2為基礎(chǔ)的高滲脫水研究模型中,有必要測得菌體基因組拷貝變化。我們通過qPCR測得在單個培養(yǎng)周期內(nèi)高滲透壓組菌體NMII10×NaCl基因組拷貝無顯著改變,而在低滲壓下NMII1/100×NaCl基因拷貝可有限增長0.7log10,同時對照組NMII基因拷貝可增加2.7log10。進(jìn)一步以第0至7 d基因拷貝繪制生長曲線,可見對比NMII的指數(shù)生長,菌體NMII10×NaCl在接種后48 h適應(yīng)性存活但未生長,相反,菌體NMII1/100×NaCl在接種后72 h開始即進(jìn)入平臺期,如圖2所示。
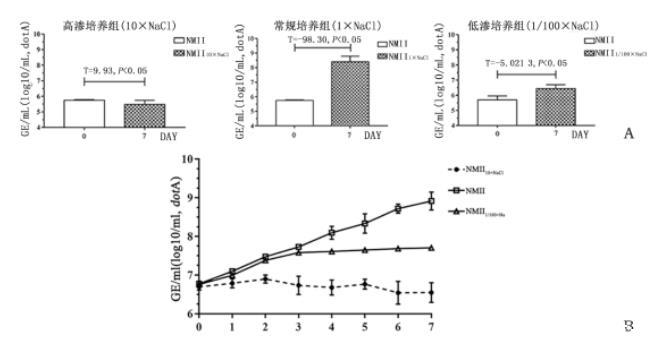
圖2貝氏柯克斯體在滲透壓梯度的無生命培養(yǎng)基中的生長特性
注:A為貝氏柯克斯體在滲透壓梯度無生命培養(yǎng)下的基因組拷貝數(shù);B為貝氏柯克斯體在滲透壓梯度培養(yǎng)條件的生長曲線
相關(guān)新聞推薦
2、基于體外重組雞傳染性貧血病毒生長曲線來研究復(fù)制效率(三)
