lmo1508/lmo1509基因缺失對單增李斯特菌生長曲線、抗氧化應激能力的影響(三)
2 結果與分析
2.1 gsh-px報告質粒的構建
利用生物信息學分析獲得gsh-px基因上游的啟動子序列,以10403S基因組和質粒pFL251為模板分別擴增出508 bp的gsh-px啟動子Pgsh-px和737 bp的gfp片段。通過SOE-PCR將Pgsh-px和gfp進行融合獲得1 245 bp的Pgsh-px-gfp片段。通過重組的方法將Pgsh-px-gfp與pERL3載體連接并構建gsh-px報告質粒pFL516。將連接產(chǎn)物用熱激法轉化至大腸桿菌DH5α感受態(tài)細胞中,挑取單克隆并使用pFL516 A/D引物對進行PCR鑒定及測序驗證,經(jīng)凝膠電泳獲得1 245 bp的條帶(圖1),符合預期大小且測序正確,說明gsh-px報告質粒成功構建。
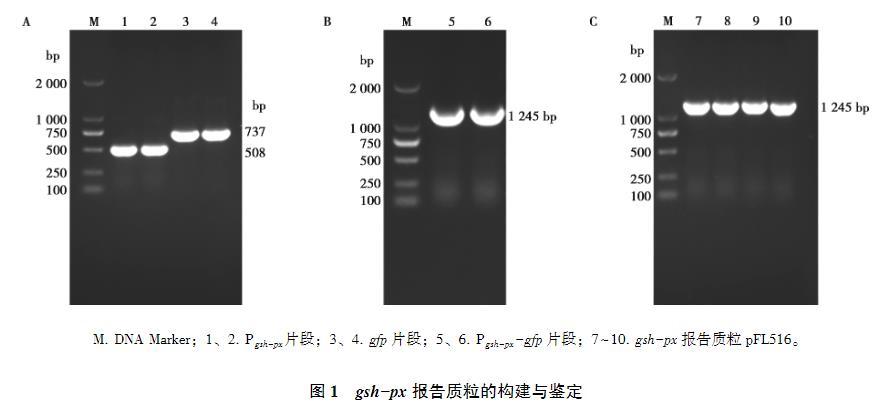
圖1 gsh-px報告質粒的構建與鑒定
2.2 熒光蛋白表達菌株的構建
提取gsh-px報告系統(tǒng)pFL516質粒,采用電轉化將pFL516電轉至LM菌株10403S感受態(tài)細胞中構建熒光蛋白表達菌株10403S-pFL516,挑取單克隆并使用pFL516 A/D引物對進行PCR鑒定,獲得pFL516目的片段(圖2),與預期結果一致,表明LM熒光蛋白表達菌株構建成功。
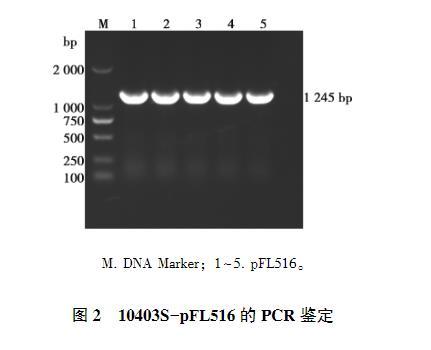
M. DNA Marker;1~5. pFL516。
圖2 10403S-pFL516的PCR鑒定
2.3 熒光蛋白表達情況
在熒光顯微鏡下,攜帶報告質粒的10403S-pFL516發(fā)出綠色熒光,而10403S無熒光(圖3 A);使用酶標儀對10403S-pFL516和10403S的熒光值進行測定,10403S-pFL516的熒光強度高達656 874 RFU,而10403S的熒光值只有9 465 RFU(圖3 B),說明該報告質粒可在LM中正常表達。
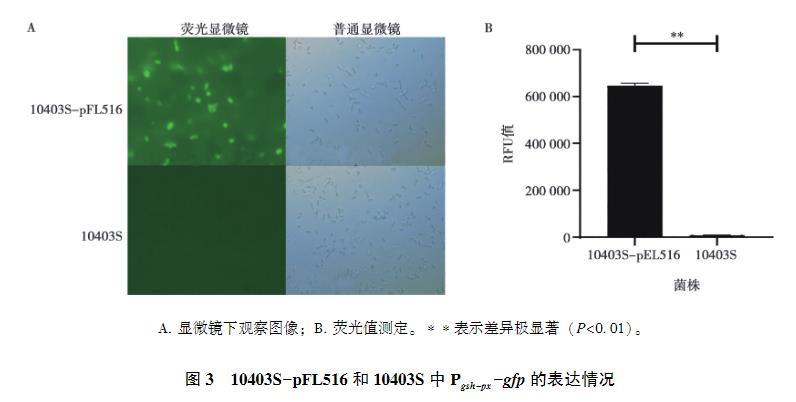
A. 顯微鏡下觀察圖像;B. 熒光值測定。表示差異極顯著(P<0.01)。
圖3 10403S-pFL516和10403S中Pgsh-px-gfp的表達情況
2.4 TCS缺失株中gsh-px報告系統(tǒng)的鑒定
將pFL516電轉入LM各TCS缺失株感受態(tài)中,涂布于EM抗性的BHI平板,挑取單菌落用pFL516 A/D引物鑒定,結果顯示報告質粒已成功電轉入TCS缺失株中(圖4)。

圖4 TCS缺失株中pFL516的PCR鑒定
2.5 TCS缺失株中熒光值的檢測
將gsh-px的報告質粒pFL516電轉入各TCS缺失株感受態(tài)中,通過檢測攜帶pFL516報告質粒的各TCS缺失株的熒光值發(fā)現(xiàn):在已敲除TCS的LM菌株中,lmo0050/lmo0051、lmo1060/lmo1061、lmo1508/lmo1509、lmo1947/lmo1948、lmo2010/lmo2011、lmo2678/lmo2679、lmo2582/lmo2583這7個TCS的缺失使得其熒光值相對于親本株10403S-pFL516極顯著升高;而lmo1021/lmo2022、lmo1377/lmo1378、lmo0691/lmo0692這3個TCS的缺失使得熒光值相對于親本株10403S-pFL516顯著降低;lmo1172/lmo1173、lmo2514/lmo2515、lmo1741/lmo1742這3個TCS的缺失使得熒光值相對于親本株10403S-pFL516極顯著降低;lmo2500/lmo2501的缺失使得其熒光值相對于親本株10403S-pFL516無顯著差異(圖5)。熒光值越大轉錄水平越高,反之則表示轉錄表達水平越低,說明lmo0050/lmo0051、lmo1060/lmo1061等7個TCS雙元調控系統(tǒng)的缺失導致gsh-px基因轉錄水平上調,它們與gsh-px啟動子之間存在負調控關系;lmo1021/lmo2022、lmo1377/lmo1378等6個TCS的缺失則導致gsh-px基因轉錄水平下調,它們與gsh-px啟動子之間存在正調控關系。
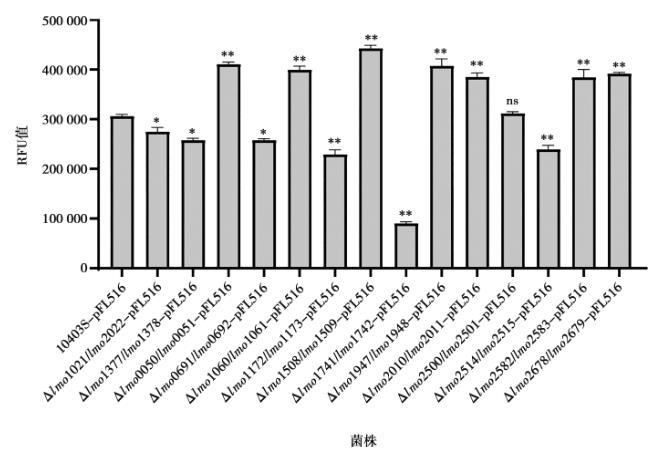
注:與對照組(10403S-pFL516)相比,ns表示差異不顯著(P>0.05),表示差異顯著(P < 0.05),*表示差異極顯著(P < 0.01)。下同。
圖5 不同TCS缺失株中gsh-px報告基因的表達水平
相關新聞推薦
1、牦牛源短小芽孢桿菌生長曲線測定及藥敏試驗、體外抑菌結果解讀(一)
2、基于可培養(yǎng)技術的古象牙病害微生物分離鑒定與抑菌劑篩選評價(三)
3、?嗜黏蛋白阿克曼菌在硫乙醇酸鹽液體培養(yǎng)基中的生長情況與代謝產(chǎn)物(一)
