基于細菌生長曲線測定探究具核梭桿菌促進肺癌發展的潛在機制(三)
2.2具核梭桿菌促進小鼠肺癌轉移
采用C57小鼠進行尾靜脈注射造模實驗,通過肺部遞送2種具核梭桿菌或PBS(圖2A)。造模成功后收集3組小鼠的肺組織,并使用IVIS Spectrum系統進行拍照(圖2B)。結果顯示,Fn-9組和Fn-ATCC組肺組織的熒光強度顯著高于PBS組(圖2C)。統計肺結節數量發現,Fn-9組和Fn-ATCC組的數量顯著高于對照組(圖2D)。同時,2組的肺器官系數也均高于PBS組(圖2E)。這些結果表明,具核梭桿菌可能促進了腫瘤細胞的增殖與轉移。
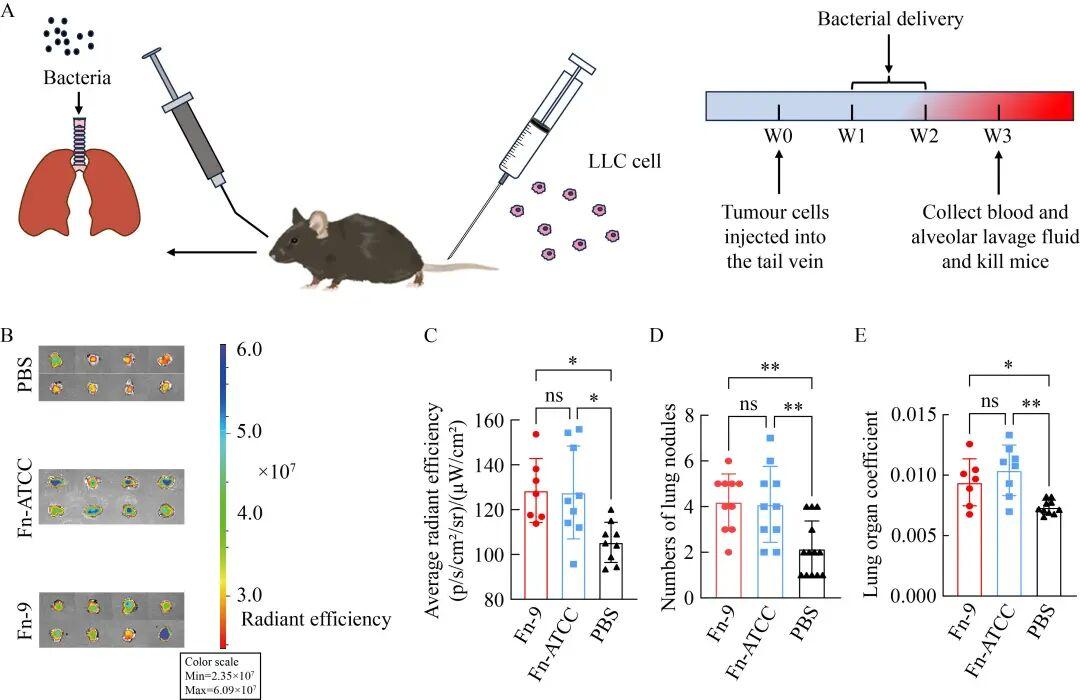
圖2具核梭桿菌促進小鼠肺癌轉移。A:實驗流程圖;B、C:Fn-9、Fn-ATCC和PBS 3組熒光強度比較;D、E:3組肺結節數量和肺器官系數。
為了進一步了解3組小鼠的肺損傷情況,對肺切片進行了HE染色分析。病理結果顯示,3組小鼠的肺部均有炎癥細胞浸潤,但Fn-9組和Fn-ATCC組的肺泡間隔破壞更為嚴重,部分氣道黏膜上皮也出現萎縮(圖3A)。值得注意的是,2組的肺腫瘤面積明顯增大,肺結節數量明顯增多(圖3A)。同樣地,qPCR檢測3組小鼠肺組織中炎癥因子的表達發現,Fn-9組和Fn-ATCC組的IL-1β和TNF-α表達量更高(圖3B、3C),而IL-6的表達在3組之間無顯著差異(圖3D)。綜上所述,在動物水平上證明了具核梭桿菌促進了肺癌的轉移和進展。
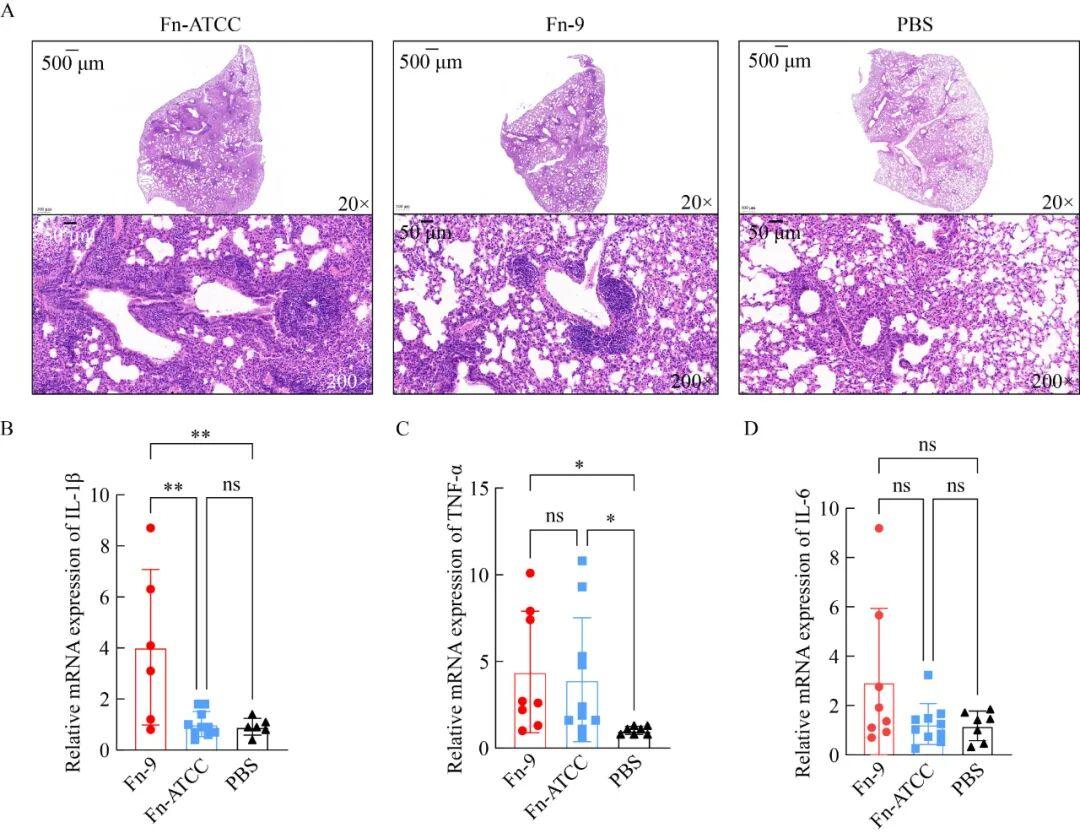
圖3病理切片圖和定量聚合酶鏈反應(qPCR)。A:Fn-9、Fn-ATCC和PBS 3組肺組織切片;B-D:IL-1β、TNF-α和IL-6在小鼠肺組織中的表達(ns:無統計學意義;*:
2.3具核梭桿菌對小鼠肺部微生物群的影響
收集上述各組及正常小鼠的肺泡灌洗液,探討具核梭桿菌對肺微生物群的影響。在屬水平,Fn-9組和Fn-ATCC組細菌組成明顯不同于PBS組(圖4A)。Chao1指數表明,Fn-9組的α多樣性顯著高于空白組(圖4B)。然而,4組間的β多樣性無顯著差異(圖4C)。MetagenomeSeq分析顯示,Fn-9組和Fn-ATCC組中Muribaculum的豐度顯著低于PBS組,而Fn-9組中Simplicispira的豐度顯著高于PBS組(圖4D)。
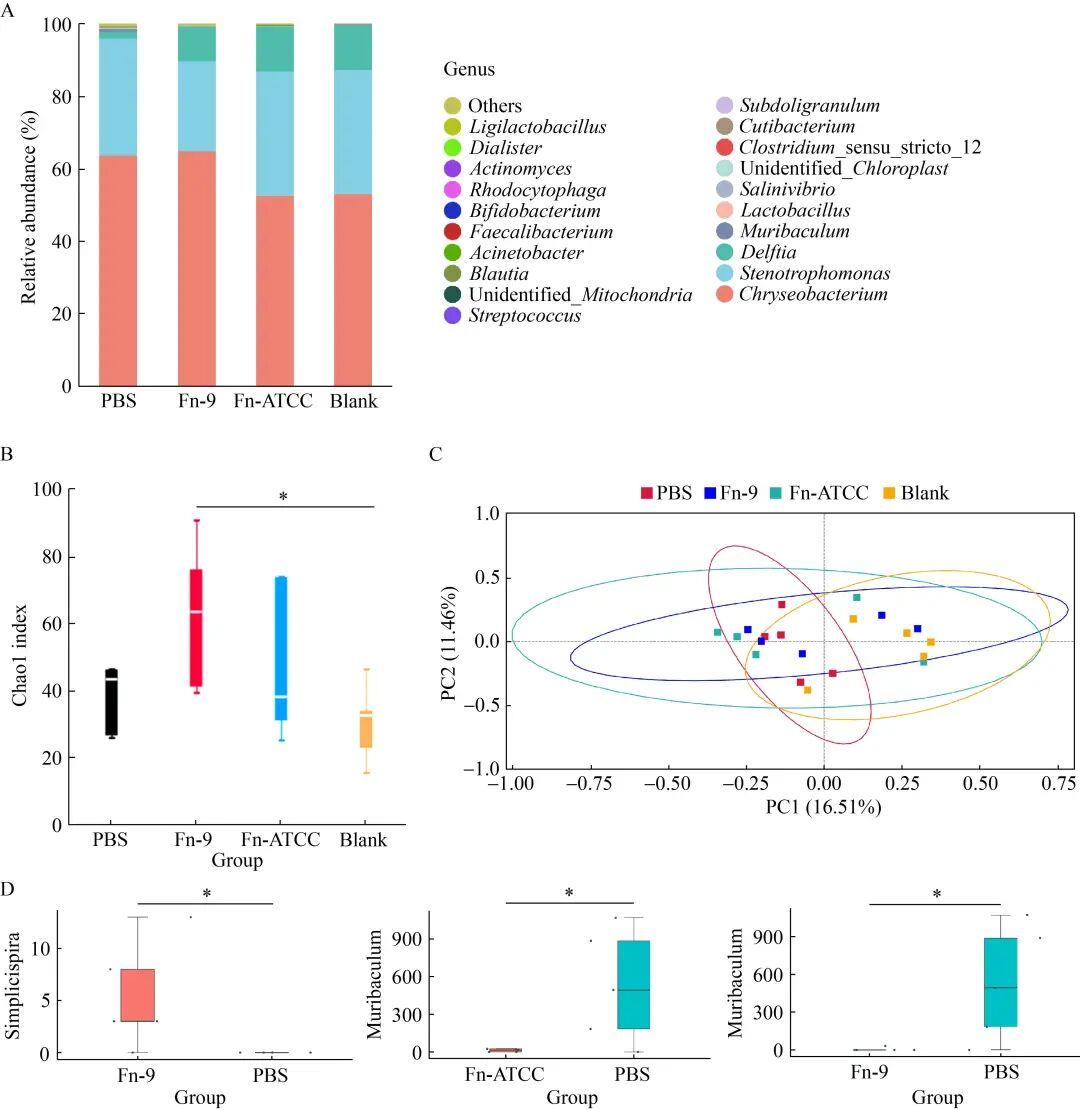
圖4具核梭桿菌對肺部微生物群的影響。A:4組菌屬水平前20個豐度的群落條形圖;B:4組肺泡灌洗液的Chao1指數(P值通過Kruskal-Wallis檢驗計算,*:P<0.05);C:4組肺泡灌洗液的PCoA圖(ANOSIM用于統計評估顯著差異);D:MetagenomeSeq檢測4組之間的差異物種(*:P<0.05)。
2.4肺組織轉錄組分析
轉錄組測序用于描述肺組織變化的特征。主成分分析(principal components analysis,PCA)結果顯示,Fn-9組、Fn-ATCC組和PBS組的轉錄組基因存在顯著差異(圖5A)。進一步通過火山圖比較其差異基因的變化,發現與PBS組相比,Fn-ATCC組共有1 855個差異基因表達上調,1 185個差異基因表達下調(圖5B);而在Fn-9組與PBS組的比較中,Fn-9組共有864個差異基因表達上調,640個差異基因表達下調(圖5C)。隨后,分析了3組小鼠肺組織中KEGG通路差異基因的富集情況。在Fn-9組、Fn-ATCC組和PBS組的比較中,差異基因主要富集在IL-17信號通路、細胞因子-細胞因子受體相互作用、細胞周期和運動蛋白等信號通路上,這提示Fn-9組和Fn-ATCC組2種菌株可能通過調節免疫反應來促進肺癌的進展(圖5D、5E)。
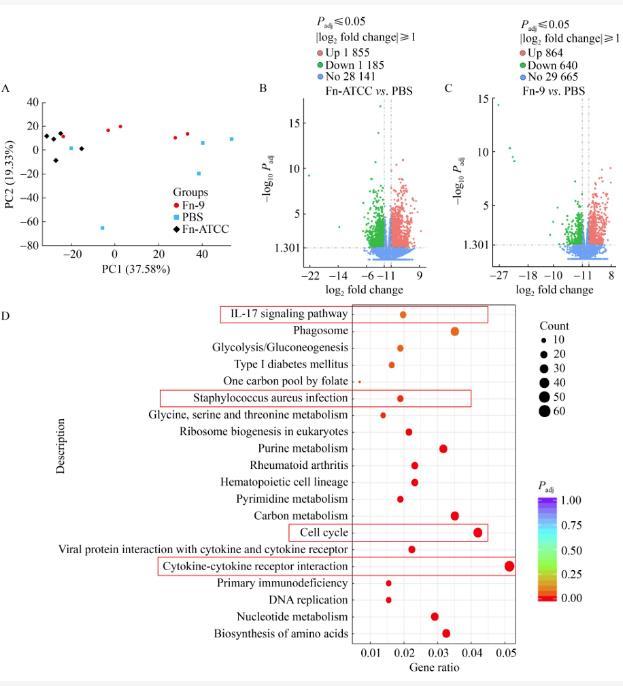
圖5感染后肺癌組織的轉錄組。A:3組樣本間的主成分分析;B、C:差異基因表達分析的火山圖;D:Fn-ATCC與PBS之間RNA-seq數據中差異基因的KEGG通路富集分析;E:Fn-9與PBS之間RNA-seq數據中差異基因的KEGG通路富集分析。
3討論與結論
傳統上,肺一直被認為是一個無菌器官,隨著分子測序技術的發展證實肺中實際上存在少量微生物,這可能是由于口腔、上呼吸道、下呼吸道和肺直接接觸導致呼吸道或口腔中的微生物進入呼吸道并在肺中定殖[12-14]。根據目前的理論,大多數微生物通過上呼吸道以及微量吸入的方式進入肺部[14-16]。相比之下,某些微生物已被證實會增加患肺癌的風險[17]。作為口腔中常見的條件致病菌,具核梭桿菌已被證明與多種疾病相關[18-20]。具核梭桿菌與牙齦卟啉單胞菌協同作用可誘發牙周炎,并促進口腔癌的發展[4,21-22]。除口腔疾病外,研究人員還在結直腸癌患者的組織中檢測到高豐度的具核梭桿菌[23-24],并進一步證實具核梭桿菌對結直腸癌有促進作用[6,25]。從作用機制上看,具核梭桿菌能激活Apcmin/+小鼠的NF-κB信號通路,并誘導TNF、IL-6、IL-8和IL-1β等促癌通路[8,26]。然而,目前尚無直接證據表明具核梭桿菌與肺癌有關。
本研究首先選擇了2種不同來源的具核梭桿菌菌株:一種是ATCC 25586標準菌株,另一種是從肺癌患者肺泡灌洗液中提取的具核梭桿菌動物亞種。與其他亞種相比,動物亞種具核梭桿菌在結直腸癌生態區域中占主導地位[27]。在動物實驗中,發現向小鼠肺部遞送具核梭桿菌可促進肺結節數量的增加,并且實驗組的肺組織在熒光成像下比對照組的熒光強度更強。通過qPCR檢測發現,小鼠肺組織中TNF-α和IL-1β基因的表達顯著增加。研究也表明,TNF-α在肺癌的上皮-間質轉化(epithelial-mesenchymal transition,EMT)、侵襲、轉移和進展過程中起著重要作用,這在TNFR2-KO小鼠植入Lewis肺癌(LLC)模型中也得到了證實[28-29]。IL-1β也被證實在腫瘤微環境中的表達升高,并在肺癌的轉移發展中發揮重要作用[30-31]。
根據肺泡灌洗液的16S rRNA基因測序結果,在實驗組和PBS組之間發現了2個不同的屬:簡單螺旋形菌屬(Simplicispira)和鼠桿狀菌屬(Muribaculum)。簡單螺旋形菌屬是一種常見于土壤、水庫和污泥中的細菌,尚未見與癌癥相關的報道[32-33]。鼠桿狀菌屬與腸道微生物群中的脂質代謝以及結直腸癌中的腸道微生物菌群失調有關[34-35]。肺組織轉錄組KEGG結果表明,具核梭桿菌可能通過免疫相關信號通路促進肺癌轉移。細胞因子-細胞因子受體相互作用通路與腫瘤密切相關,研究證實齊墩果酸可通過調節細胞因子-細胞因子受體相互作用通路來調控乳酸菌抑制腫瘤的發展,TRIM6也通過該通路促進膠質瘤的發展[36-37]。同樣地,TNF信號通路也參與了細胞凋亡及其對癌癥疾病的影響[38-39]。具核梭桿菌進入小鼠肺部后,激活了金黃色葡萄球菌感染途徑,而金黃色葡萄球菌具有很強的促炎能力,能引起肺炎等疾病[40-41]。肺部炎癥會誘發肺部微環境的改變,從而導致肺癌病變[42]。此外,盡管在結直腸癌研究中已顯示具核梭桿菌能夠進入腸上皮細胞發揮作用,但對于具核梭桿菌是否能進入肺上皮細胞尚無相關報道,這也是后續機制研究的方向之一。
綜上所述,通過細胞實驗驗證了具核梭桿菌能促進A549細胞的增殖和轉移,并通過體內實驗進一步驗證了它能促進肺癌的轉移和惡化。根據16S rRNA基因測序結果和肺組織轉錄組結果,具核梭桿菌進入小鼠肺部后擾亂了肺部菌群的組成,激活了肺組織中多個與炎癥和免疫相關的信號通路,這可能是具核梭桿菌促進肺癌的潛在機制。
相關新聞推薦
1、基于ELISA和細菌生長曲線應用的結合定量檢測腸炎沙門氏菌(二)
2、基于微生物生長曲線監測系統探究肺炎克雷伯菌菌株毒力與碳青霉烯類耐藥性的關系(二)
