鴨瘟病毒基因缺失株rDEV-ΔVP26生長曲線、蝕斑面積及免疫原性分析(二)
1.5重組病毒的拯救
參照磷酸鈣轉(zhuǎn)染方法將pDEV-ΔVP26轉(zhuǎn)染至CEFs,待其出現(xiàn)熒光且熒光斑達(dá)到90%后收獲病毒,命名為rDEV-ΔVP26。
1.6重組病毒生長曲線
將CEFs傳代于12孔板上,次日分別用0.01 MOI(multiplicity of infection)的rDEV-EF1和rDEV-ΔVP26感染CEFs,2 h后加入含有2%FBS的DMEM,重復(fù)3孔后置于37℃CO2培養(yǎng)箱培養(yǎng)。分別于感染后12、24、36、48、60、72、84、96 h收集3孔細(xì)胞和上清混合后研磨,分裝,置于-80℃保存。采用Reed-Muench法在含有CEFs的96孔板測定各個時間點(diǎn)的TCID50,并繪制出重組病毒的生長曲線。
1.7重組病毒蝕斑面積
將rDEV-EF1和rDEV-ΔVP26病毒凍存液用不同稀釋度進(jìn)行稀釋,接種于12孔板中的單層CEFs上,2 h后,換上含有1.5%甲基纖維素的DMEM培養(yǎng)基,置于37℃CO2培養(yǎng)箱培養(yǎng)48 h。在熒光顯微鏡下各拍攝100個熒光蝕斑,采用Image J軟件測量蝕斑面積并取平均值。用SPSS 11.5軟件的One-way ANOVA程序進(jìn)行統(tǒng)計(jì)學(xué)分析。
1.8 Western blot方法檢測蛋白表達(dá)
分別收集rDEV-EF1和rDEV-ΔVP26感染細(xì)胞樣品,加入上樣緩沖液混勻,100℃加熱10 min,離心,取10μL蛋白上清液于蛋白預(yù)制膠(10%~20%)電泳,電泳時制備雙份,電泳完畢,分別轉(zhuǎn)印至小孔徑NC膜(0.22μm)和NC膜(0.45μm),放入封閉液中4℃封閉過夜。以小鼠源抗VP26多克隆抗體(1∶500稀釋)或小鼠抗UL19蛋白多克隆抗體(1∶500)作為一抗,HRP標(biāo)記的山羊抗小鼠IgG(1∶1 000稀釋)作為二抗于37℃孵育1 h,PBST洗滌完畢后,加入ECL化學(xué)發(fā)光試劑作用5 min,最后于凝膠成像系統(tǒng)下曝光顯色。
1.9 UL35基因缺失病毒的安全性分析
將40只30日齡無DEV抗體的麻鴨隨機(jī)分為5組,每組8只并飼養(yǎng)于不同欄舍。每組麻鴨分別在腿部肌肉注射1 mL 1×105 TCID50的rDEV-ΔVP26、rDEV-EF1和1 mL 1×106 TCID50的rDEV-ΔVP26、rDEV-EF1,對照組注射1 mL DMEM。觀察2周,記錄各組鴨的狀態(tài)、發(fā)病和死亡情況來評價(jià)rDEV-ΔVP26對鴨的安全性。
1.10 UL35基因缺失病毒的免疫原性分析
將48只30日齡無DEV抗體的麻鴨隨機(jī)分為6組,每組8只,各組分欄舍飼養(yǎng)。每組麻鴨腿部肌肉分別注射1 mL 1×104 TCID50 rDEV-ΔVP26、rDEV-EF1和1 mL 1×105 TCID50 rDEV-ΔVP26、rDEV-EF1,對照組注射1 mL DMEM,留1組作為陰性對照組(NC組),不做任何處理。免疫14 d后用鴨瘟強(qiáng)毒CHv株(100倍鴨半數(shù)致死劑量,100 DLD50)對免疫組和DMEM對照組采用肌肉注射的方式進(jìn)行攻毒,NC組不做任何處理。于2周內(nèi)觀察各組鴨的狀態(tài)、發(fā)病和死亡情況,通過各組發(fā)病、存活情況來評價(jià)rDEV-ΔVP26對鴨瘟強(qiáng)毒株的免疫保護(hù)情況。試驗(yàn)過程中所有死亡鴨立即進(jìn)行剖檢、觀察鴨各臟器病變和進(jìn)行PCR檢測。
1.11數(shù)據(jù)的統(tǒng)計(jì)與分析
采用GraphPad Prism 5軟件的t檢驗(yàn)(Student′s t test)比較各組之間的差異性,ns.無顯著差異;*.P<0.05表示差異顯著;**.P<0.01、***.P<0.001、****.P<0.000 1均表示差異極顯著。
2結(jié)果
2.1 UL35基因缺失突變體克隆的PCR鑒定
抽提重組BACs克隆,以其為模版、ΔVP26-JD-F/ΔVP26-JD-R為引物對進(jìn)行PCR擴(kuò)增,結(jié)果表明UL35基因按照預(yù)期缺失(圖1)。
M.2000 bp相對分子質(zhì)量標(biāo)準(zhǔn)(2 000、1 000、750、500、250、100);1.pDEV-EF1(949 bp);2.pDEV-ΔVP26-Kan(1 634 bp);3.pDEV-ΔVP26(595 bp)
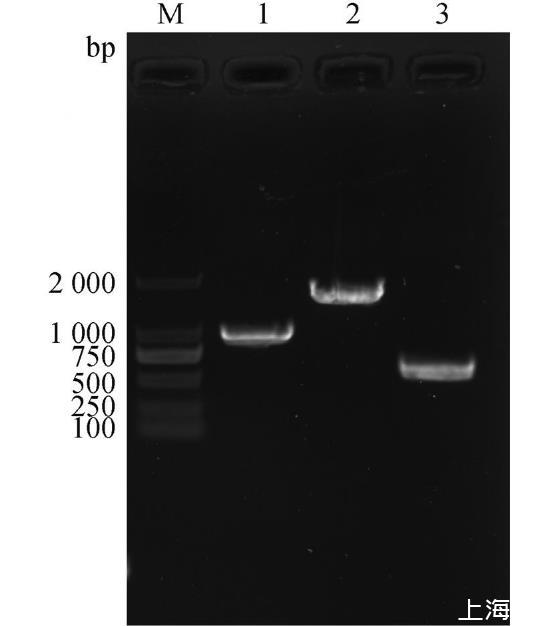
圖1 UL35基因缺失突變體克隆的PCR鑒定
2.2 UL35基因缺失突變體病毒的拯救和鑒定
以pDEV-ΔVP26質(zhì)粒轉(zhuǎn)染CEFs細(xì)胞后24 h,在熒光顯微鏡下可以見到綠色熒光蝕斑(圖2),表明成功拯救了UL35基因缺失病毒rDEV-ΔVP26。rDEV-ΔVP26可以在CEFs細(xì)胞上增殖和形成蝕斑,說明UL35基因不是DEV在細(xì)胞上增殖所必需的。抽提病毒DNA,以ΔVP26-JD-F/ΔVP26-JD-R引物對進(jìn)行PCR擴(kuò)增,再次驗(yàn)證UL35基因缺失成功(圖3A)。采用Western blot方法對rDEV-ΔVP26感染細(xì)胞中VP26蛋白的表達(dá)進(jìn)行檢測,發(fā)現(xiàn)VP26蛋白成功缺失,而對照組rDEV-EF1感染細(xì)胞內(nèi)正常表達(dá)。且兩組樣品都能檢測到病毒主要衣殼蛋白UL19(圖3B)。

圖2拯救的重組病毒rDEV-ΔVP26(100×)、對照病毒rDEV-EF1(100×)和正常細(xì)胞對照
M1.2 000 bp相對分子質(zhì)量標(biāo)準(zhǔn)(2 000、1 000、750、500、250、100);1.rDEV-EF1(949 bp);2.rDEV-ΔVP26(595 bp);M2.蛋白質(zhì)相對分子質(zhì)量標(biāo)準(zhǔn)
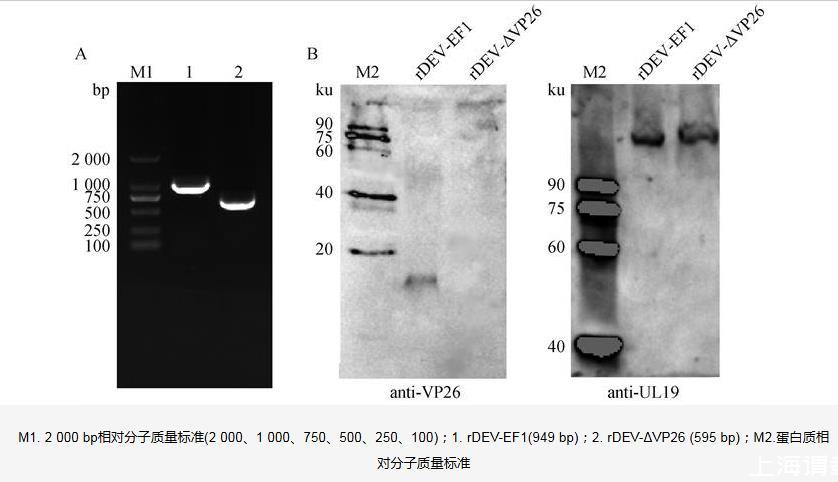
圖3 PCR方法(A)和Western blot法(B)驗(yàn)證rDEV-ΔVP26病毒UL35缺失
相關(guān)新聞推薦
1、氣單胞菌所屬科、流行病學(xué)特點(diǎn)、耐藥率分析
2、枯草芽孢桿菌BC80-6發(fā)酵培養(yǎng)基、生長條件及對煙草根黑腐病菌生防作用(二)
3、草魚呼腸孤病毒培養(yǎng)與滴度測定、及在草魚、CIK細(xì)胞上的生長特性研究(三)
